ポリープ状脈絡膜血管症に対するアイリーア(2mg)の有効性と安全性:PLANET試験
(日本人部分集団解析を含む2年成績)
PLANET試験(日本人を含む第Ⅲb/Ⅳ相国際共同試験)

- 1)
- Lee WK, et al.: JAMA Ophthalmol. 2018; 136: 786-793.
- 2)
- Wong TY, et al.: Am J Ophthalmol. 2019; 204: 80-89.
- 3)
- Ogura Y, et al.: Jpn J Ophthalmol. 2021; 65: 344-353.
本ページでは「アイリーア(2mg)」を「アイリーア」と記載しています。
試験概要1、2)
目的
PCV患者における、アイリーア(2mg)単独療法の有効性および安全性を、アイリーア(2mg)+光線力学的療法(レスキューPDT)と比較検討する。
試験デザイン
96週間、二重遮蔽、偽治療対照、無作為化、第Ⅲb/Ⅳ相試験
試験対象
以下に該当する患者333例(うち、日本人は159例)
- PCVと診断された50歳以上の患者
- 病変最大径(GLD)が5,400μm未満であるか9乳頭面積(DA)未満の患者
- 最高矯正視力(BCVA)がETDRSで73~24文字の患者
投与方法
- 本試験は以下の期間により構成される。
導入期:0~8週目
無作為割り付け:12週目
治療継続期:12~52週目[アイリーア(2mg)2q8±レスキュー治療]、52~96週目(T&E※1±レスキュー治療) - 導入期にはすべての患者にアイリーア(2mg)の毎月投与を3回行う。
- 12週目にアイリーア(2mg)単独療法群、PDT併用療法群のいずれかに1:1の割合で無作為に割り付ける。その際、12週時点でレスキュー治療が必要と評価された患者、および日本人患者が均等に含まれるように割り付ける。(12週時点でレスキュー治療が必要となる患者が各群50名程度であると想定)
- レスキュー治療が不要と評価された患者には52週目までアイリーア(2mg)を8週ごとに投与する。
- 12週目以降、レスキュー治療が必要と評価された患者には、アイリーア(2mg)単独療法群ではアイリーア(2mg)の4週ごと投与とシャムPDTによるレスキュー治療を、PDT併用療法群ではアイリーア(2mg)4週ごと投与と実薬PDTによるレスキュー治療を行う。
評価項目
<主要評価項目>
- 52週時におけるBCVAのベースラインからの変化量
<副次評価項目>
- 52週時におけるベースラインから15文字以上の視力低下がみられなかった患者の割合
<探索的評価項目>
- 96週時におけるBCVAのベースラインからの変化量
- 96週時におけるベースラインから15文字以上の視力低下がみられなかった患者の割合
- 52週時および96週時におけるCSTのベースラインからの変化量
- 52週時および96週時におけるポリープ状病巣の完全退縮率
- アイリーア(2mg)およびPDTによる治療回数
- レスキュー治療を必要とした患者の割合 など
<安全性評価項目>
- すべての有害事象、TEAE、重篤な有害事象、APTC定義に基づく動脈血栓塞栓事象、死亡 など
<事前に規定された評価項目(部分集団解析)>
- レスキュー治療の有無別でみたBCVAのベースラインからの変化量
- 日本人集団における上記のすべての有効性評価項目、および安全性評価項目 など
解析計画
<検証的な解析(第1種の過誤を考慮し、検出力を考慮し例数設計された解析)>
- 主要評価項目(FAS):アイリーア(2mg)単独療法のPDT併用療法に対する非劣性の検証。変化量の最小二乗平均の群間差[アイリーア(2mg)単独療法群-PDT併用療法群]の両側95%信頼区間を、ベースライン値を共変量とし、投与群、民族、および12週目におけるレスキュー治療の有無を固定効果とした共分散分析により求める。(非劣性限界値:ETDRS‒5文字)
<第1種の過誤を考慮した解析(検出力を考慮した例数設計はされていない)>
- 副次評価項目(FAS):アイリーア(2mg)単独療法のPDT併用療法に対する非劣性の検討。主要評価項目の検証により非劣性が認められた場合に、ベースラインからETDRS15文字以上の視力低下がみられなかった患者の割合を確認し、群間差の95%信頼区間を人種/民族および12週目におけるレスキュー治療の有無により調整されたCochran-Mantel-Haenszel検定により求める。(非劣性限界値:‒7%)
<探索的な解析>
- 探索的評価項目(FAS)、安全性評価項目(SAF)、部分集団解析(FAS)
- なお、欠損値の代入にはLOCFを用いる。
利益相反
本試験および本論文の執筆・編集はBayer AG, Berlin の資金提供により行われた。
著者のうち2名はBayerの社員であり、その他の著者にBayerおよび参天製薬より助成金、個人的報酬を受領している者が含まれる。
※1:治験担当医の裁量により、1週または2週単位で投与間隔を延長する任意T&E
ETDRS:early treatment diabetic retinopathy study T&E:treat and extend CST(central subfield macular thickness):中心サブフィールド網膜厚
TEAE(treatment-emergent adverse event):治療下で発現した有害事象 APTC:antiplatelet trialists’ collaboration
FAS(full analysis set):最大の解析対象集団 SAF(safety analysis set):安全性解析対象集団
LOCF(last observation carried forward):最終評価スコア外挿法
試験デザイン1)
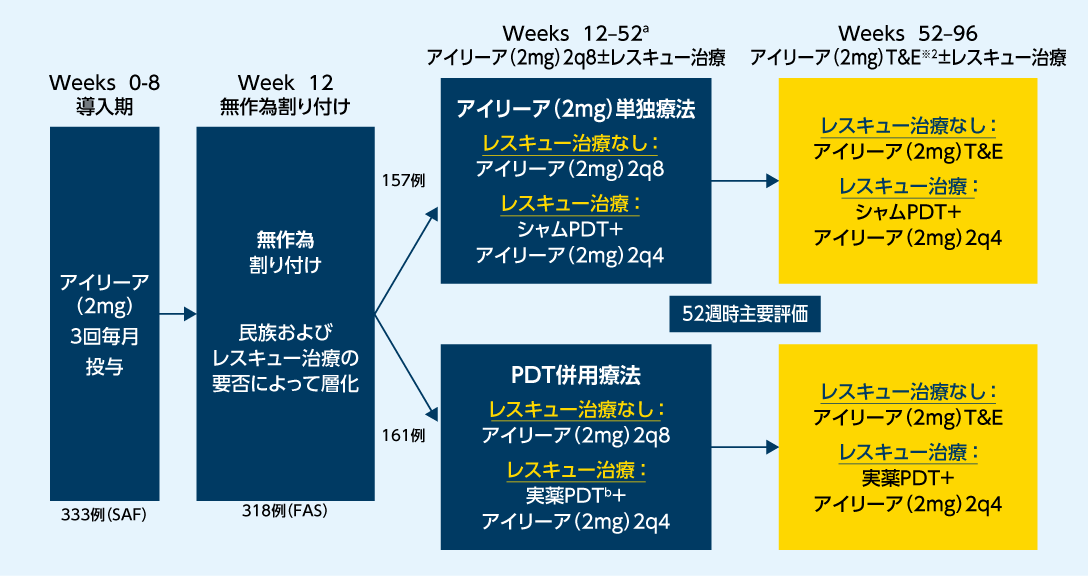
a:レスキュー基準の評価 b:ベルテポルフィン6mg/m2静脈内投与
PDT(実薬またはシャム)はレスキュー基準に該当する場合にのみ、各国の添付文書にそって施行
※2:治験担当医の裁量により、1週または2週単位で投与間隔を延長する任意T&E
文献1)より一部改変
ベースラインの患者背景(全集団)1)
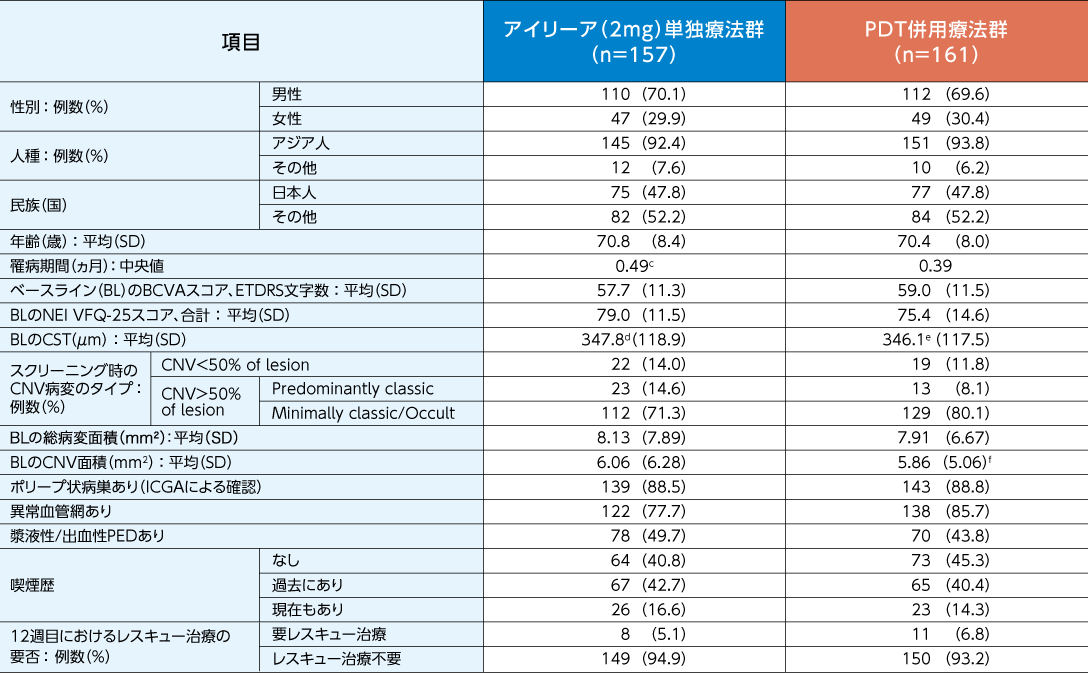
c:n=156 d:n=152 e:n=158 f:n=160
SD(standard deviation):標準偏差 ICGA(indocyanine green angiography):インドシアニングリーン蛍光眼底造影
PED(pigment epithelial detachment):網膜色素上皮剥離 NEI VFQ-25:25-item National Eye Institute Visual Function Questionnaire
<主要評価項目>
BCVAの変化量は、52週時にアイリーア(2mg)単独療法群のPDT併用療法群に対する非劣性が検証されました
BCVAのベースラインからの変化量の推移(全集団*1)1、2)
FAS(LOCF)
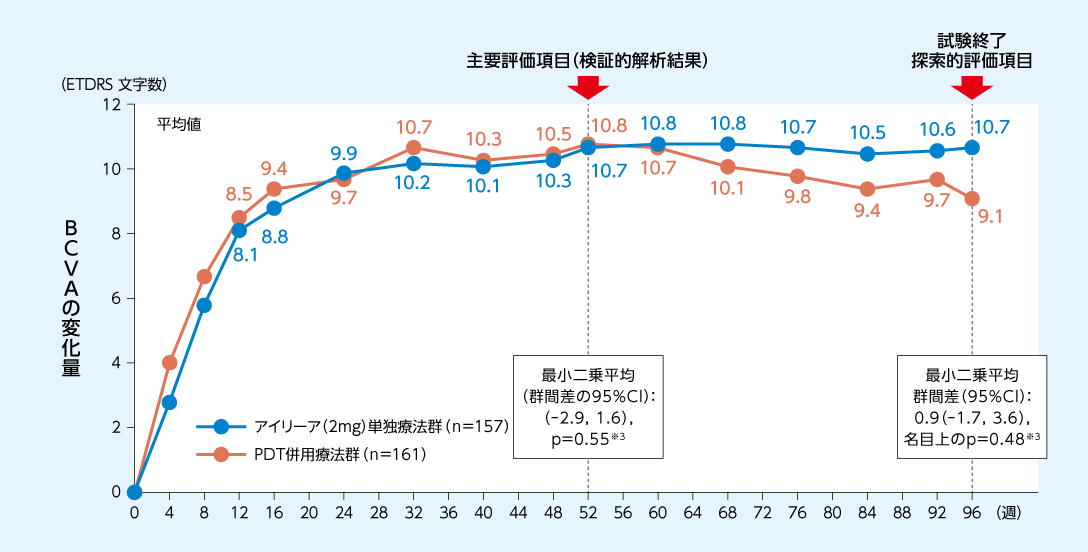
*1:
アイリーア(2mg)単独療法群、PDT併用療法群のいずれも、要レスキュー治療群、レスキュー治療不要群を含む。
※3:
ベースライン値を共変量とし、投与群、人種/民族および12週目におけるレスキュー治療の有無を固定効果とした共分散分析
52週時における非劣性限界値:ETDRS-5文字
<副次評価項目>
15文字以上の視力低下がみられなかった患者の割合について、52週時にアイリーア(2mg)単独療法群のPDT併用療法群に対する非劣性が示されました
15文字以上の視力低下がみられなかった患者の割合(全集団*2)1、2)
FAS(LOCF)
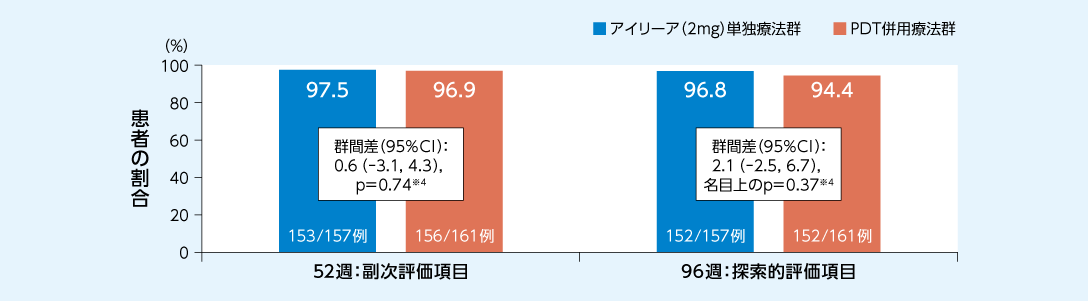
*2:
アイリーア(2mg)単独療法群、PDT併用療法群のいずれも、要レスキュー治療群、レスキュー治療不要群を含む。
※4:
人種/民族および12週目におけるレスキュー治療の有無により調整されたCochran-Mantel-Haenszel検定
52週時における非劣性限界値:-7%
文献1、2)より作図
レスキュー治療基準1)

*3:
アイリーア(2mg)2q4+実薬またはシャムPDT
<探索的評価項目>
96週間を通じてレスキュー治療を必要とした患者の割合はアイリーア(2mg)単独療法群で15.9%、PDT併用療法群で18.0%でした
レスキュー治療を必要とした患者の割合1、2)
FAS(LOCF)
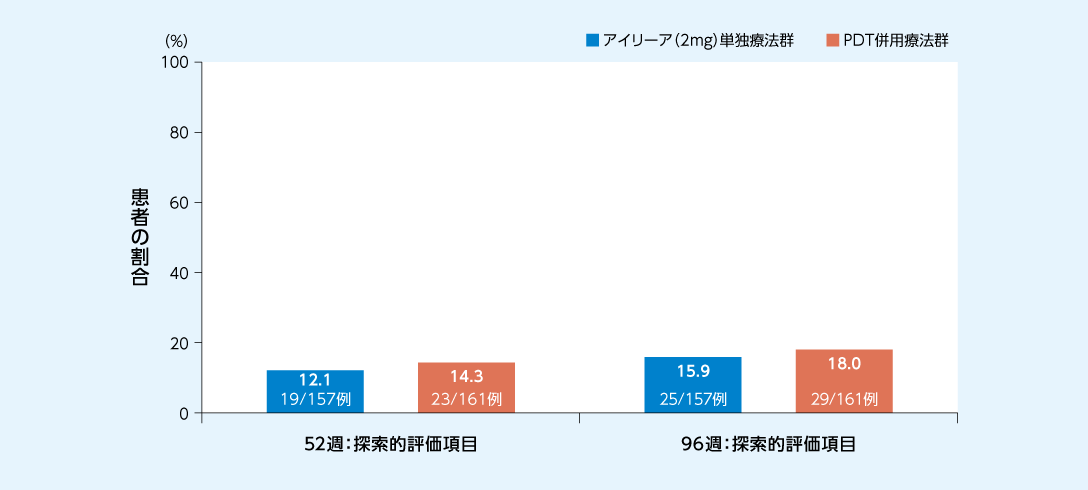
文献1、2)より作図
<部分集団解析:レスキュー治療なし>
レスキュー治療を必要としなかった患者サブグループにおける96週時のBCVA変化量はアイリーア(2mg)単独療法群で+12.3文字、PDT併用療法群で+11.1文字でした
BCVAのベースラインからの変化量の推移1、2)
FAS(LOCF)
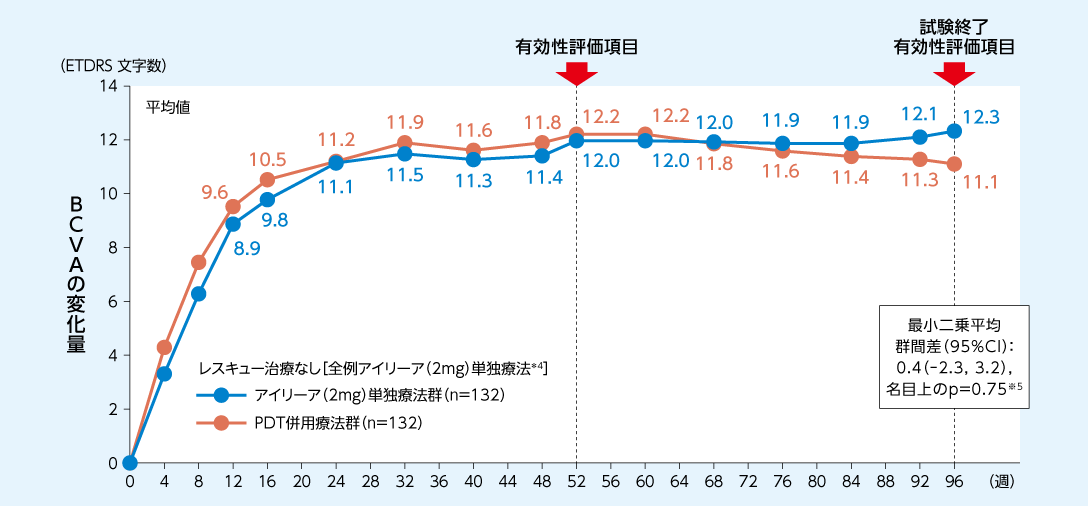
*4:
レスキュー治療不要群ではPDT(実薬またはシャム)は施行されなかった。患者は割り付けられた治療群を問わずアイリーア(2mg)単独療法を受けた。
※5:
ベースライン値を共変量とし、投与群、人種/民族および12週目におけるレスキュー治療の有無を固定効果とした共分散分析
<部分集団解析:レスキュー治療あり>
レスキュー治療を必要とした患者サブグループにおける96週時のBCVA変化量はアイリーア(2mg)単独療法群で+2.6文字、PDT併用療法群で0文字でした
BCVAのベースラインからの変化量の推移1、2)
FAS(LOCF)
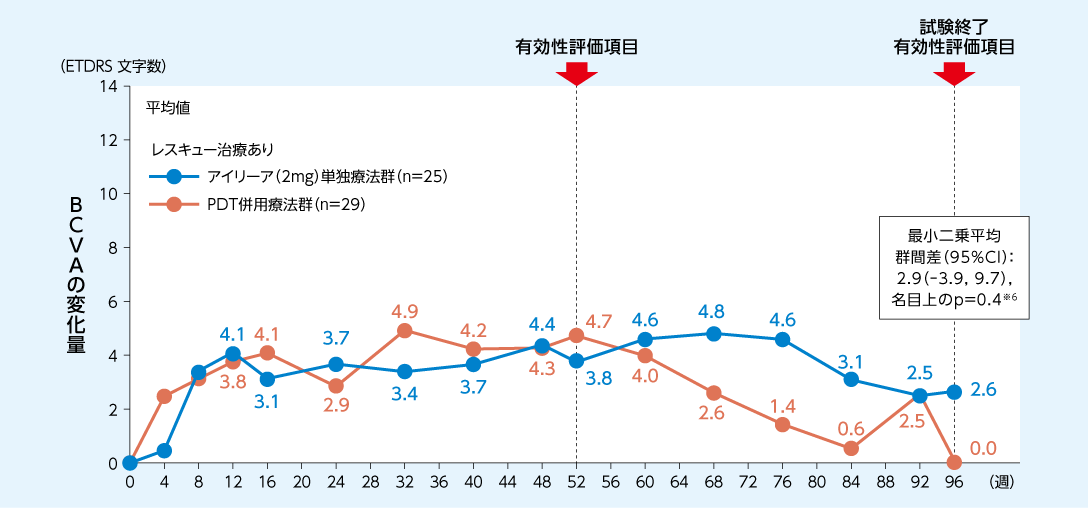
※6:
ベースライン値を共変量とし、投与群、人種/民族および12週目におけるレスキュー治療の有無を固定効果とした共分散分析
<探索的評価項目>
96週時におけるCSTの変化量はアイリーア(2mg)単独療法群で-140.0μm、PDT併用療法群で-135.4μmでした
CSTのベースラインからの変化量の推移(全集団*5)1、2)
FAS(LOCF)
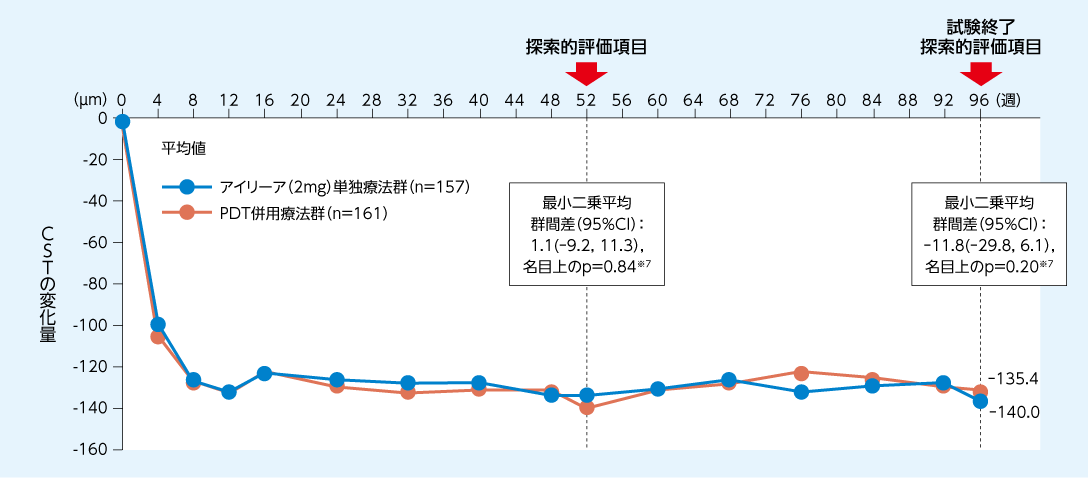
*5:
アイリーア(2mg)単独療法群、PDT併用療法群のいずれも、要レスキュー治療群、レスキュー治療不要群を含む。
※7:
ベースライン値を共変量とし、投与群、人種/民族および12週目におけるレスキュー治療の有無を固定効果とした共分散分析
<探索的評価項目>
96週時におけるポリープ状病巣の完全退縮率はアイリーア(2mg)単独療法群で33.1%、PDT併用療法群で29.1%でした
ポリープ状病巣の完全退縮※8が得られた患者の割合(全集団*6)1、2)
FAS(OC)
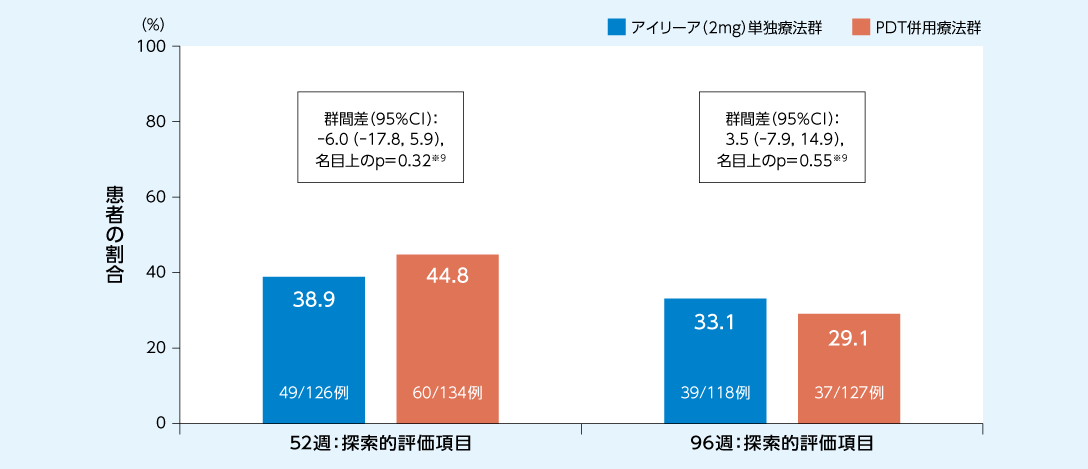
ベースラインにおいてポリープが認められた患者のうち、52週目に評価できなかった患者を除く。
*6:
アイリーア(2mg)単独療法群、PDT併用療法群のいずれも、要レスキュー治療群、レスキュー治療不要群を含む。
※8:
ICGAでポリープ状病巣が認められない患者
※9:
人種/民族および12週目におけるレスキュー治療の有無により調整されたCochran-Mantel-Haenszel検定
OC:
observed cases
<探索的評価項目>
96週間のアイリーア(2mg)の平均投与回数はアイリーア(2mg)単独療法群で12.7回、PDT併用療法群で12.6回でした
治療回数(全集団*7)2)
FAS
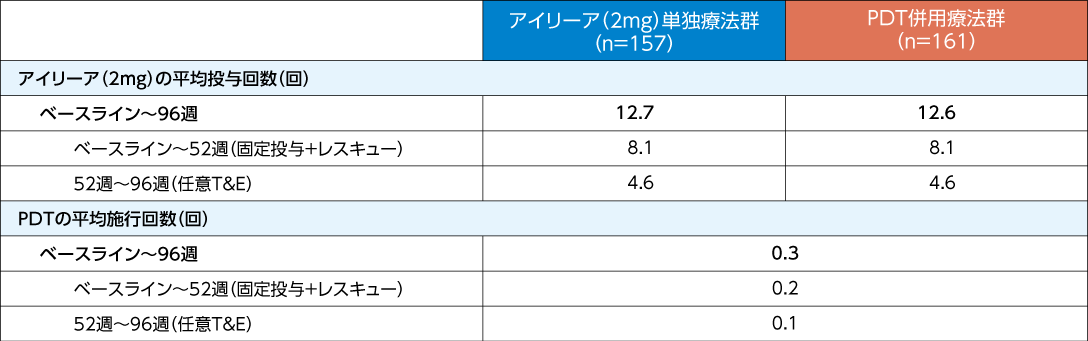
*7:
アイリーア(2mg)単独療法群、PDT併用療法群のいずれも、要レスキュー治療群、レスキュー治療不要群を含む。
文献2)より作表
<安全性評価項目>
すべての有害事象はアイリーア(2mg)単独療法群157例中114例(72.6%)、PDT併用療法群161例中110例(68.3%)に認められました
安全性(96週)2)
SAF
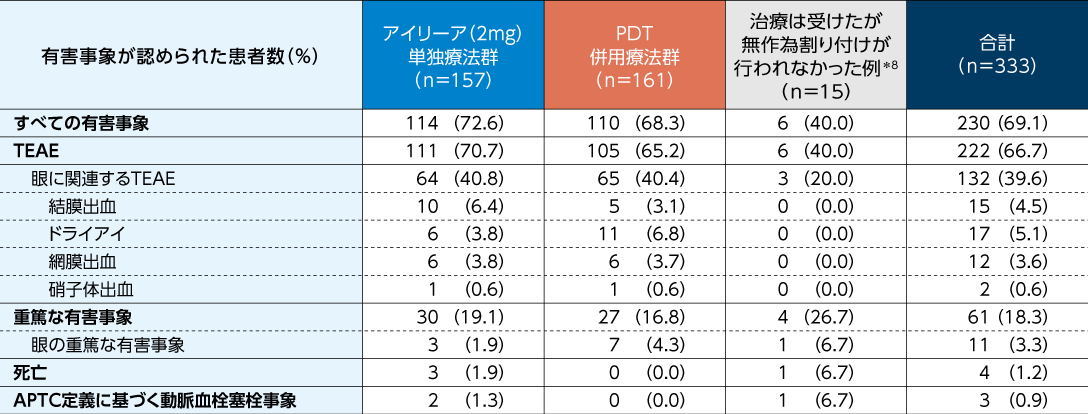
最も発現頻度の高かった有害事象は、アイリーア(2mg)単独療法群では結膜出血(6.4%)、PDT併用療法群ではドライアイ(6.8%)であった。
- アイリーア(2mg)投与に関連する重篤な有害事象として、アイリーア(2mg)単独療法群で狭心症、不安定狭心症、不整脈、冠状動脈狭窄症、白内障、上部消化管出血が各1例ずつ、PDT併用療法群で網膜動脈分枝閉塞症(BRAO)が1例、治療は受けたが無作為割り付けが行われなかった例*8で心臓突然死が1例に認められた。
- ベルテポルフィン投与に関連する重篤な有害事象として、PDT併用療法群で視力低下が1例に認められた。
- 投与中止に至ったアイリーア(2mg)投与に関連する有害事象としてBRAO、RPE tearが各1例ずつ、ベルテポルフィン投与に関連する有害事象として視力低下が1例に認められた。
(PLANET試験 社内資料)
*8:
治療を受けたが、プロトコルの逸脱、有害事象、脱落、死亡、または追跡不能により12週目に無作為化されなかったすべての患者
患者背景とベースライン特性(日本人集団)3)
FAS
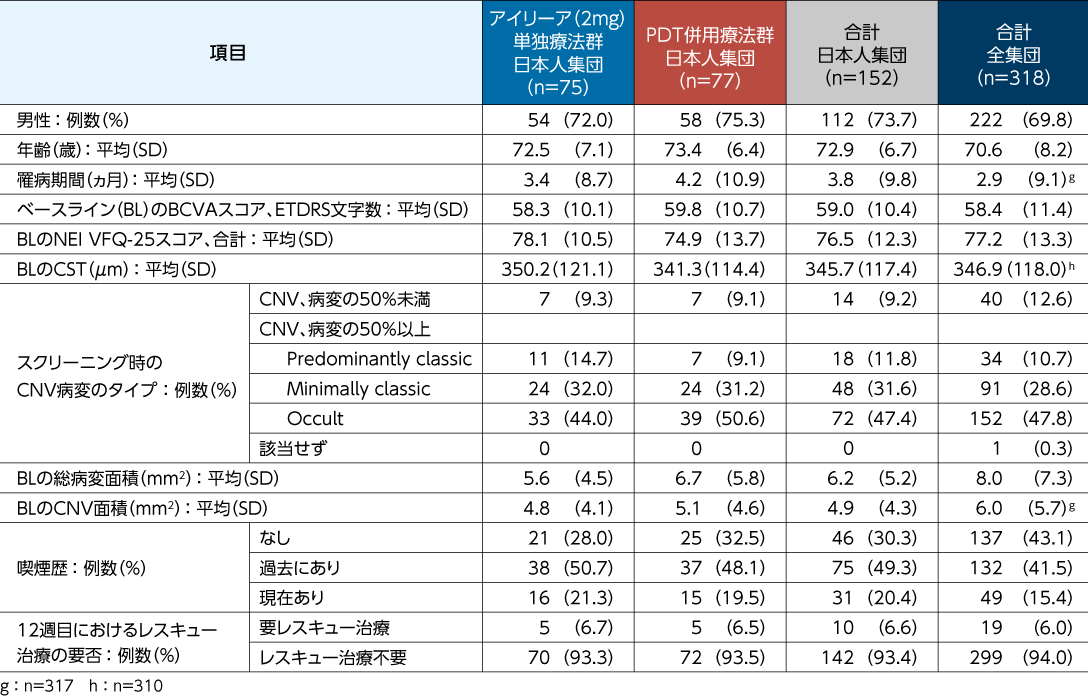
<部分集団解析:日本人>
96週時におけるBCVAの変化量は日本人集団のアイリーア(2mg)単独療法群で+9.7文字、PDT併用療法群で+9.5文字でした
BCVAのベースラインからの変化量の推移3)
FAS(LOCF)
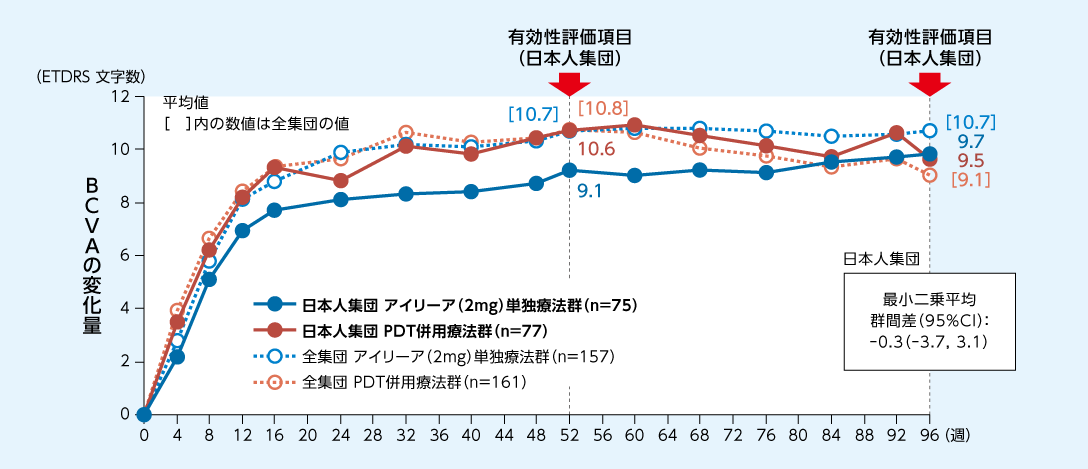
全集団、日本人集団ともに、アイリーア(2mg)単独療法群、PDT併用療法群のいずれも、要レスキュー治療群、レスキュー治療不要群を含む。
<部分集団解析:日本人>
96週時に15文字以上の視力低下がみられなかった患者の割合は日本人集団のアイリーア(2mg)単独療法群で97.3%、PDT併用療法群で96.1%でした
15文字以上の視力低下がみられなかった患者の割合(96週時)3)
FAS(LOCF)
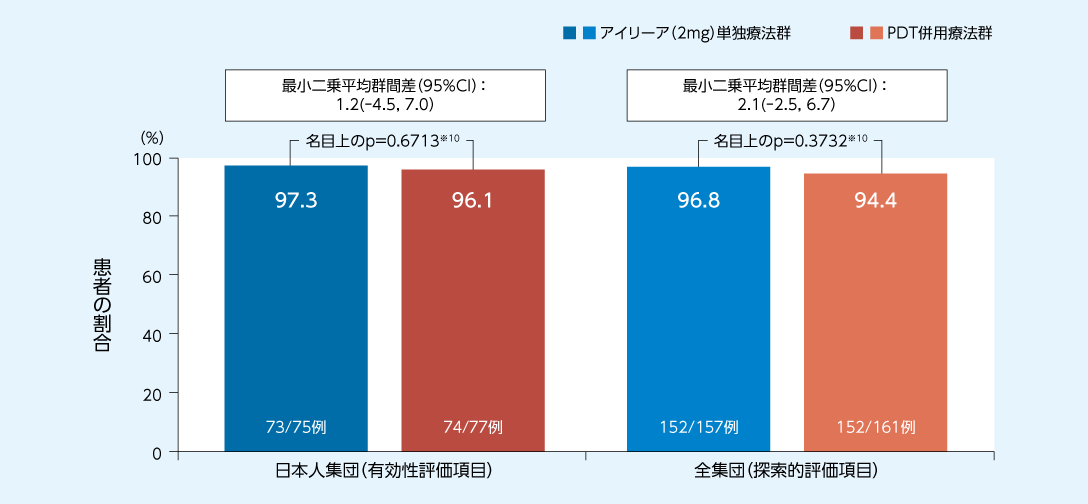
※10
Cochran‒Mantel‒Haenszel検定
<部分集団解析:日本人、レスキュー治療あり>
日本人集団における96週間を通じてレスキュー治療を必要とした患者の割合はアイリーア(2mg)単独療法群で18.7%、PDT併用療法群で15.6%でした
レスキュー治療を必要とした患者の割合(96週)3)
FAS
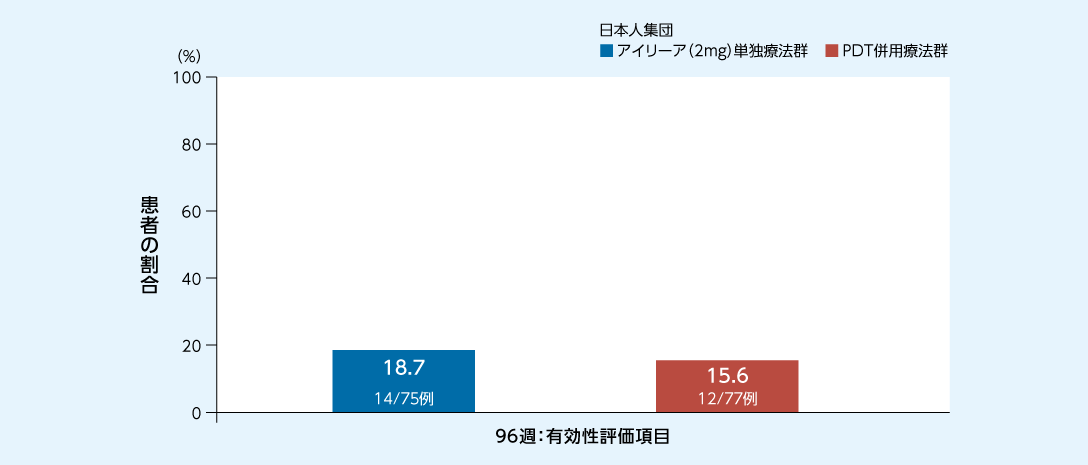
文献3)より作図
<部分集団解析:日本人>
日本人集団におけるポリープ状病巣の完全退縮率はアイリーア(2mg)単独療法群が52週時で35.3%、96週時で25.0%、PDT併用療法群がそれぞれ35.2%、37.9%でした
ポリープ状病巣の完全退縮※12が得られた患者の割合3)
FAS(OC)
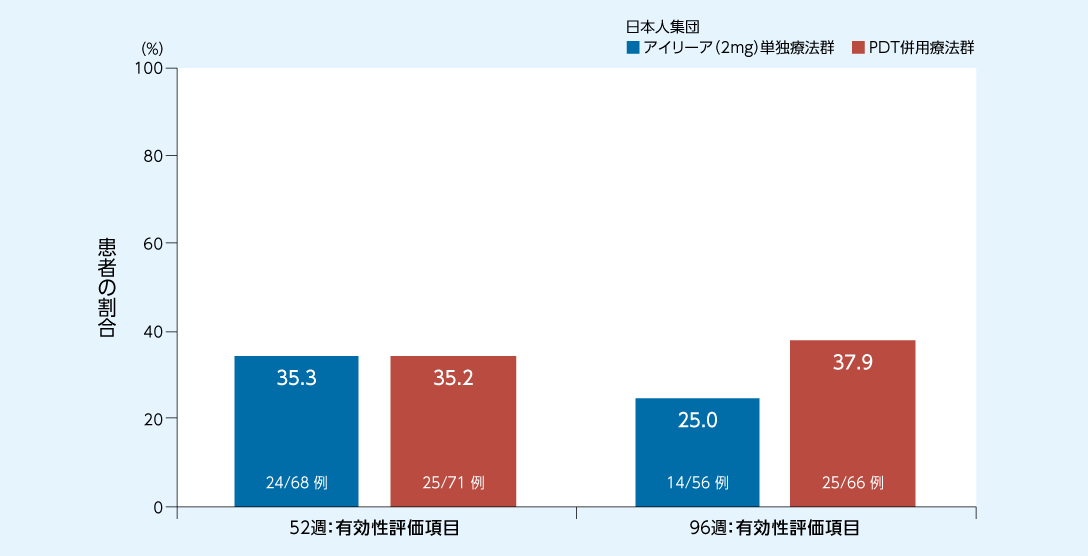
※11
ICGAでポリープ状病巣が認められない患者
<部分集団解析:日本人>
日本人集団における96週間のアイリーア(2mg)の平均投与回数はアイリーア(2mg)単独療法群で12.6回、PDT併用療法群で12.4回、PDT平均施行回数はそれぞれ0.4回、0.2回でした
治療回数3)
FAS
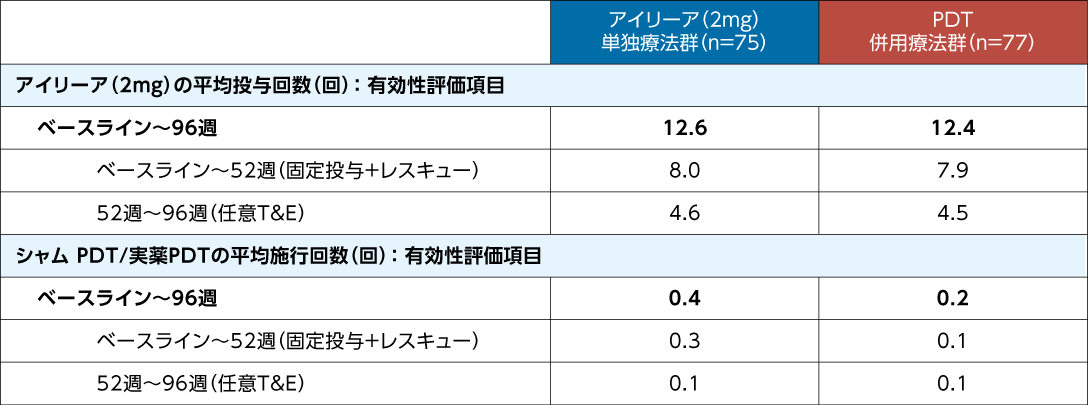
文献3)より作表
<部分集団解析:日本人>
日本人集団において、すべての有害事象はアイリーア(2mg)単独療法群75例中59例(78.7%)、PDT併用療法群77例中57例(74.0%)に認められました
安全性(96週:日本人集団)3)
SAF
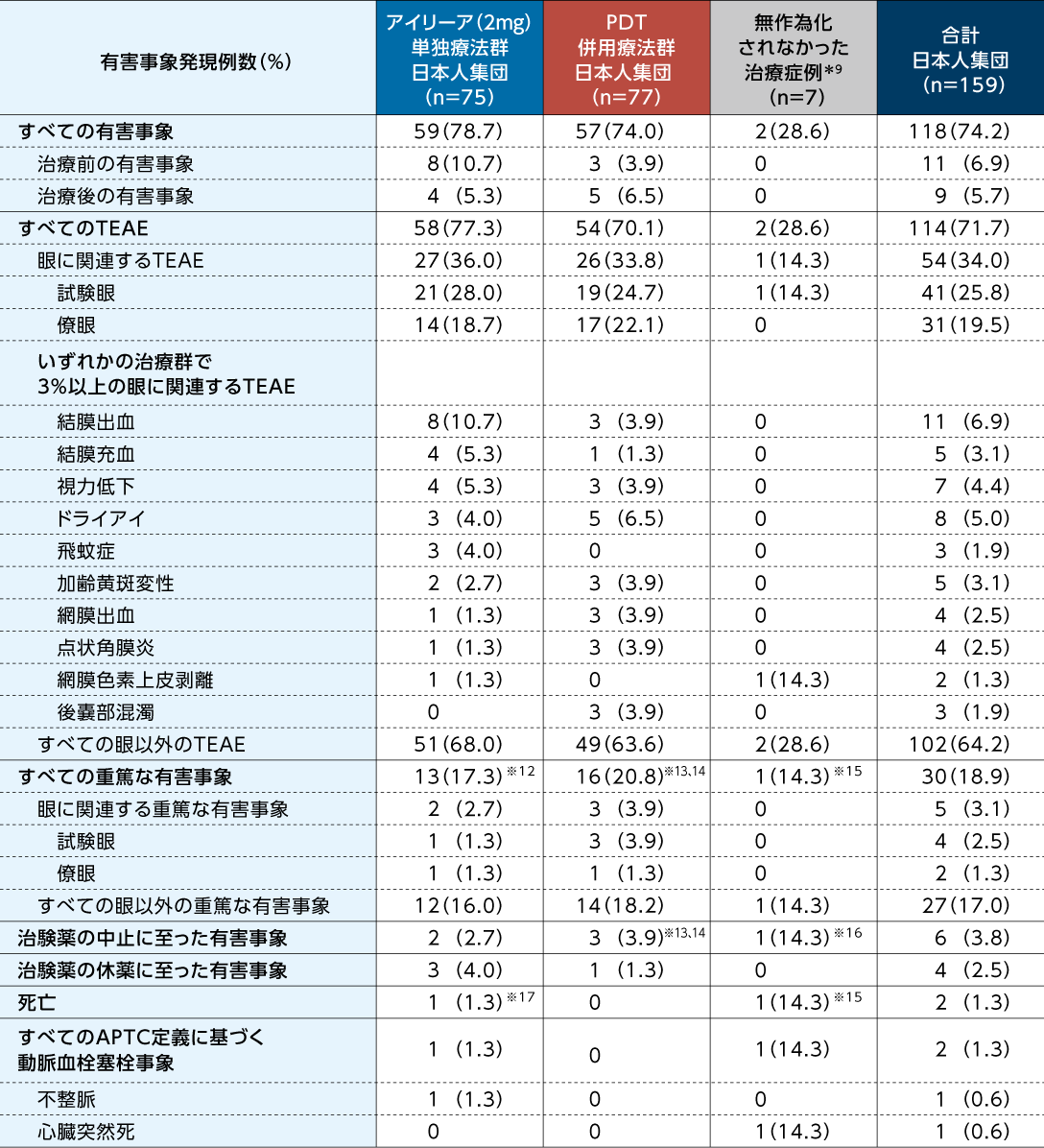
アイリーア(2mg)投与(手技を含む)に関連する有害事象
※12:
不整脈1例、上部消化管出血1例、冠状動脈狭窄症・白内障1例(2件)
※13:
網膜動脈分枝閉塞症(BRAO)1例
※15:
心臓突然死 1例
※16:
RPE tear 1例
※17:
不整脈1例
ベルテポルフィン投与(手技を含む)に関連する有害事象
※14:
視力低下1例
(PLANET試験 社内資料)
*9:
治療を受けたが、プロトコルの逸脱、有害事象、脱落、死亡、または追跡不能により12週目に無作為化されなかったすべての患者



