副作用注)一覧表
注) 投与手技に起因する有害事象を含む。
国内外で実施された第Ⅲ相試験(12試験※)において報告された副作用



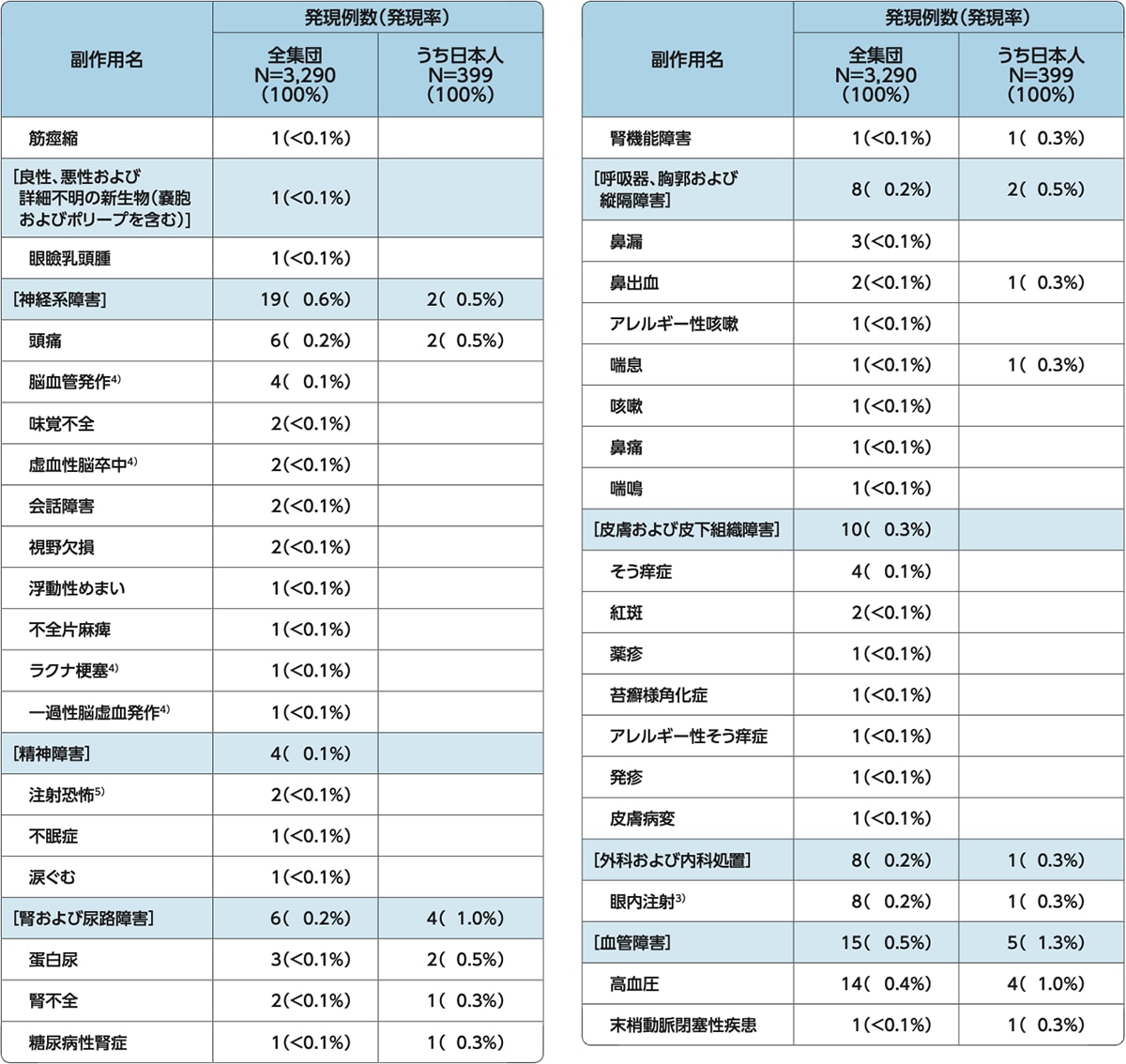
(MedDRA Ver. 23.1)
- 滲出型加齢黄斑変性(AMD)患者を対象とした試験:VIEW1、VIEW2
網膜中心静脈閉塞症(CRVO)に伴う黄斑浮腫を有する患者を対象とした試験:GALILEO、COPERNICUS
網膜静脈分枝閉塞症(BRVO)に伴う黄斑浮腫を有する患者を対象とした試験:VIBRANT
病的近視における脈絡膜新生血管(mCNV)を有する患者を対象とした試験:MYRROR
糖尿病黄斑浮腫(DME)を有する患者を対象とした試験:VISTA-DME、VIVID-DME、VIVID-Japan
血管新生緑内障(NVG)患者を対象とした試験:VEGA、VENERA
未熟児網膜症(ROP)患者を対象とした試験:FIREFLEYE
- 1)
- 「白内障」、「皮質白内障」、「核性白内障」、「嚢下白内障」、「水晶体混濁」をグループ化し、うち「投与手技との因果関係が否定できない有害事象(治験薬との因果関係は問わない)」を「外傷性白内障」の事象名で、「投与手技との因果関係は否定できるが治験薬との因果関係は否定できない有害事象」を「白内障」の事象名でまとめて集計し、重大な副作用とその他の副作用にそれぞれ記載した。
- 2)
- [黄斑変性]:本剤の適応症のうち、AMDの原疾患(悪化も含む)とした。
- 3)
- [過量投与、眼内注射]:過量投与と適用上の注意の項にそれぞれ記載した。
- 4)
- [脳血管発作、虚血性脳卒中、ラクナ梗塞、一過性脳虚血発作]をまとめて「脳卒中」の事象名で集計し〔0.2%(8例/3,290例)〕、重大な副作用に記載した。
- 5)
- [注射恐怖]:AMD、CRVOに伴う黄斑浮腫およびmCNVのCTDの副作用一覧表では「針恐怖」と分類されていた。電子添文のその他の副作用では、「針恐怖」と記載。



