日本人を含む第Ⅲ相国際共同試験:PULSAR試験1)
(アフリベルセプト2mgに対する非劣性の検証)
1)バイエル薬品社内資料[日本人を含む第Ⅲ相国際共同試験:PULSAR試験]承認時評価資料
高濃度製剤を用いてより高用量のアフリベルセプトを硝子体内投与したときのシミュレーション(ヒト硝子体内における遊離型アフリベルセプト濃度-時間プロファイルを1-コンパートメントモデルにより推定†)では、アフリベルセプト8mgの硝子体内投与により、既承認のアフリベルセプト2mg硝子体内投与と比較して投与間隔を約20日(2半減期)延長できると予測されたことから、海外第Ⅱ相試験(CANDELA試験2))が実施され、さらに、本試験において、アイリーア8mgの用法及び用量を「8mgを4週間隔で連続3回投与後、12週間隔で硝子体内投与する群」および「8mgを4週間隔で連続3回投与後、16週間隔で硝子体内投与する群」の2群に設定し、アフリベルセプト2mgに対する非劣性を検証しました。
† 照会事項への回答
2)バイエル薬品社内資料[海外第Ⅱ相試験:CANDELA試験]承認時参考資料
【実施地域】アジア太平洋地域(日本含む)、オーストラリア、欧州、中東、南米、北米の27ヵ国、251施設
試験概要
目的
中心窩下CNVを伴うnAMD患者を対象に、アイリーア8mg12週間隔または16週間隔投与による有効性についてアフリベルセプト2mg8週間隔投与に対する非劣性を検証するとともに、安全性についても検討する
試験対象
中心窩下CNVを伴うnAMD患者1,011例(うち日本人:98例)
[主な選択基準]
- 試験眼において評価されたnAMDに続発する中心窩下CNVの活動性病変(中心窩に影響を及ぼす傍中心窩病変を含む)を有する50歳以上の男女
- 試験眼の総CNV病変面積(classicおよびoccultの両CNV病変を含む)が病変全体の50%を超える
- 試験眼のETDRS視力表による最高矯正視力文字数が78〜24文字(スネレン視力で20/32〜20/320)であり、nAMDが主な原因であると判断される最高矯正視力文字数の減少がある
- OCTで、試験眼の中心窩領域(中心窩から直径1mmの範囲)に影響を及ぼすIRFおよび/またはSRFが認められる など
[主な除外基準]
- 試験眼に、nAMD以外の原因によるCNVを有する
- 試験眼に、蛍光眼底造影により評価した総病変面積が12視神経乳頭面積(12視神経乳頭面積は30.5mm2とし、病変には出血、瘢痕、新生血管を含む)を超える
- 試験眼にコントロール不良の緑内障(抗緑内障薬による治療にもかかわらず眼圧が25mmHgを超える場合)を有する
- 試験眼に特発性または自己免疫性ぶどう膜炎の既往歴を有する
- スクリーニング来院前12週以内に、いずれかの眼に、眼内の炎症または感染を有する
- 試験眼に対する血管新生阻害薬による治療歴を有する
- いずれかの眼における、糖尿病網膜症、糖尿病黄斑浮腫またはnAMD以外の網膜血管疾患の既往歴または臨床所見を有する
- コントロール不良の高血圧(収縮期血圧160mmHg超または拡張期血圧95mmHg超)を有する
- スクリーニング来院前24週以内に脳血管発作または心筋梗塞の既往歴を有する など
試験デザイン
無作為化二重遮蔽実薬対照比較試験
投与方法
対象患者をアフリベルセプト2mg8週間隔投与群、アイリーア8mg12週間隔投与群、アイリーア8mg16週間隔投与群の3群に1:1:1の比で無作為に割り付け※1、硝子体内投与した。試験薬の投与は片眼のみに実施した。
- 2mg8週間隔投与群:アフリベルセプト2mgを4週間隔で連続3回投与後、8週間隔で投与※2
- 8mg12週間隔投与群:アイリーア8mgを4週間隔で連続3回投与後、12週間隔で投与※3
- 8mg16週間隔投与群:アイリーア8mgを4週間隔で連続3回投与後、16週間隔で投与※3,4
ただし、8mg12週間隔投与群および16週間隔投与群では、16週目以降、DRM基準※5,6に従い投与間隔を変更した。

※1
地域(日本、その他の地域)およびベースラインの最高矯正視力文字数(60文字未満、60文字以上)に基づき層別化した。
※2
試験期間を通じて8週間隔で投与を継続した。
※3
16週目または20週目にDRM基準(短縮)を満たした場合、当該来院日に投与を行い、以降は8週間隔に短縮した。24週目以降のアイリーア投与来院日にDRM基準(短縮)を満たした場合は次回投与間隔を4週幅で短縮した。52週目以降は、1年目と同一のDRM基準(短縮)に加えて、DRM基準(延長)に従い、基準を満たした場合は投与間隔を4週幅で短縮または延長した。なお、8週間隔を最短の投与間隔とした。
※4
16週目または20週目にDRM基準(短縮)を満たさず、24週目にDRM基準(短縮)を満たした場合は、当該来院日に投与を行い、以降は12週間隔に短縮した。
※5
DRM基準(短縮:16週目以降):「最高矯正視力文字数の12週目からの5文字超低下」かつ「CRTの12週目からの25μm超増加、または中心窩に新たな出血、または新たな新生血管が発現」
※6
DRM基準(延長:52週目以降):「最高矯正視力文字数の12週目からの低下が5文字未満」かつ「OCTで中心窩領域に滲出液が認められない」かつ「中心窩に新たな出血および新生血管の発現がない」
主な有効性評価項目
主要評価項目:
48週目における最高矯正視力文字数のベースラインからの変化量
主な副次評価項目:
- 60週目における最高矯正視力文字数のベースラインからの変化量
- 16週目に中心窩領域にIRFおよびSRFが認められなかった患者の割合
その他の副次評価項目:
- 48週目に中心窩領域にIRFおよびSRFが認められなかった患者の割合
- 48週目におけるCRTのベースラインからの変化量 など
探索的評価項目:
- 8mg12週間隔投与群において48週目および60週目まで投与間隔が12週間隔以上であった患者の割合
- 8mg16週間隔投与群において48週目および60週目まで投与間隔が16週間隔以上であった患者の割合
- その他の副次評価項目(48週目の評価)に設定した評価項目の60週目の評価 など
主な安全性評価項目
有害事象、副作用、重篤な有害事象、投与中止に至った有害事象、死亡、眼内炎症反応、眼圧上昇事象、眼圧上昇の程度、高血圧事象、APTC 定義による動脈血栓塞栓事象 など
事前に規定されたその他の評価項目
- 8mg12週間隔投与群および8mg16週間隔投与群において16週目または20週目に投与間隔が8週間隔へ短縮となった患者の割合
- 8mg12週間隔投与群および8mg16週間隔投与群において48週目および60週目までにいずれかの時点で投与間隔が短縮となった患者の割合
- 8mg12週間隔投与群において48週目および60週目に次回予定された投与間隔が12週間隔以上であった患者の割合
- 8mg16週間隔投与群において48週目および60週目に次回予定された投与間隔が16週間隔以上であった患者の割合
- 48週目および60週目までの投与回数 など
解析計画
主要評価項目および主な副次評価項目において、検定全体のfamily-wiseの第1種の過誤確率を0.025(片側検定)に制御した。主要評価項目および主な副次評価項目における検定の多重性の調整には、下記の階層的検定手順を用い、より上位の階層にランク付けされた仮説を棄却した後にのみ、有意水準0.025(片側)で続く下位の仮説の検定を可能とした※。

いずれも2mg8週間隔投与群に対する比較検定
階層的検定手順に基づく仮説はすべての患者が60週目を完了(または早期中止)した後に評価した。
主要評価項目を含む48週目までの有効性評価について、60週目完了後のデータによる再解析は実施しなかった。
※ ⑥において優越性が示されなかったため、検定を終了した。
検証的な解析(第1種の過誤を考慮し、検出力を考慮し例数設計された解析)
主要評価項目(FAS):
8mg12週間隔投与群および8mg16週間隔投与群の2mg8週間隔投与群に対する非劣性の検証(非劣性限界値-4文字)
第1種の過誤を考慮した解析(検出力を考慮した例数設計はされていない)
主な副次評価項目(FAS):
「60週目における最高矯正視力文字数のベースラインからの変化量」は主要評価項目と同一の方法により解析
「16週目に中心窩領域にIRFおよびSRFが認められなかった患者の割合」は8mg投与群併合の2mg8週間隔投与群に対する優越性の検討
探索的な解析
その他の副次評価項目(FAS)
探索的評価項目(FAS、SAF)
事前に規定されたその他の評価項目(SAF)
部分集団解析:日本人の部分集団解析 など
CNV(choroidal neovascularization):脈絡膜新生血管、ETDRS(Early Treatment Diabetic Retinopathy Study):糖尿病網膜症早期治療研究、OCT(optical coherence tomography):光干渉断層計、
IRF(intraretinal fluid):網膜内液、SRF(subretinal fluid):網膜下液、DRM(dose regimen modification):用法用量変更、APTC(Antiplatelet Trialists’ Collaboration)
● 中心窩領域:中心窩から直径1mmの範囲
● CRT(central retinal thickness):中心網膜厚(中心窩領域の網膜厚)
● FAS(full analysis set):最大の解析対象集団。無作為化され、少なくとも1回の試験薬投与を受けたすべての患者。無作為割り付けされた群に基づき解析を行った。
● SAF(safety analysis set):安全性解析対象集団。無作為化され、少なくとも1回の試験薬投与を受けたすべての患者。実際の投与に基づき解析を行った。
試験対象例数と各群の患者の内訳

※
うち4例は米国のHIPAA(医療保険の携行性と責任に関する法律)に関する署名が得られなかったため、データベースから除外し、1,011例を解析対象とした。
患者背景および特性(FAS)
PULSAR試験において、各群のベースライン時の人口統計学的特性および疾患特性は以下の通りでした。

※1
読影施設で評価した
※2
適切な装置を有する施設においてインドシアニングリーン蛍光眼底造影により任意で評価した
※3
フルオレセイン蛍光眼底造影/眼底撮影を用いて評価した
PCV(polypoidal choroidal vascularization):ポリープ状脈絡膜血管症、RAP(retinal angiomatous proliferation):網膜血管腫状増殖
視力評価
最高矯正視力文字数のベースラインからの変化量[48週:主要評価項目(検証的解析結果)]
48週目における最高矯正視力文字数のベースラインからの変化量(最小二乗平均値)は、8mg12週間隔投与群で+6.1文字、8mg16週間隔投与群で+5.9文字、2mg8週間隔投与群で+7.0文字でした。8mg12週間隔投与群および8mg16週間隔投与群と2mg8週間隔投与群の群間差(両側95%信頼区間)はそれぞれ-1.0(-2.9, 0.9)文字、-1.1(-3.0, 0.7)文字であり、8mg12週間隔投与群および8mg16週間隔投与群と2mg8週間隔投与群の群間差の95%信頼区間の下限が非劣性限界値(-4文字)を上回ったことから、8mg12週間隔投与群および8mg16週間隔投与群の2mg8週間隔投与群に対する非劣性が検証されました。
最高矯正視力文字数のベースラインからの変化量[60週:主な副次評価項目]
60週目における最高矯正視力文字数のベースラインからの変化量(最小二乗平均値)について、8mg12週間隔投与群および8mg16週間隔投与群と2mg8週間隔投与群の群間差の95%信頼区間の下限が非劣性限界値(-4文字)を上回ったことから、8mg12週間隔投与群および8mg16週間隔投与群の2mg8週間隔投与群に対する非劣性が示されました。
最高矯正視力文字数のベースラインからの変化量(MMRM、FAS)

※1 実測値 ※2 各群‒2mg8週間隔投与群 ※3 非劣性(非劣性限界値‒4文字)の片側検定
階層的検定手順に従い、下位の「8mg投与群併合の中心窩領域にIRFおよびSRFが認められなかった患者の16週目における優越性」は示されたが、続く「8mg12週間隔投与群の最高矯正視力の48週目における優越性」が示されなかったため、検定を終了した。
最高矯正視力文字数のベースラインからの変化量の推移(MMRM、FAS)

●
MMRM(mixed model for repeated measurements):反復測定混合効果モデル。ベースラインの最高矯正視力文字数を共変量、投与群、来院および層別因子[地域(日本、その他の地域)、ベースラインの最高矯正視力文字数(60文字未満、60文字以上)]を固定効果とし、ベースラインの最高矯正視力文字数と来院の交互作用項、投与群と来院の交互作用項を含む。
最高矯正視力文字数が69文字以上であった患者の割合
[48週:その他の副次評価項目、60週:探索的評価項目]
最高矯正視力文字数が69文字以上であった患者の割合は、48週目では8mg12週間隔投与群で56.9%、8mg16週間隔投与群で54.3%、2mg8週間隔投与群で57.9%でした。また、60週目ではそれぞれ56.3%、54.6%、58.2%でした。
最高矯正視力文字数が69文字(スネレン視力で20/40)以上であった患者の割合(LOCF、FAS)

※
各群‒2mg8週間隔投与群[地域(日本、その他の地域)およびベースラインの最高矯正視力文字数(60文字未満、60文字以上)で層別化したMantel-Haenszel型の重みを用いて調整した]
●
LOCF(Last Observation Carried Forward):最終評価スコア外挿法。欠測値に対して欠測前の最後の測定値を用いて補完する解析方法
36週目から48週目および48週目から60週目までの
最高矯正視力文字数の平均値のベースラインからの変化量[探索的評価項目]
36週目から48週目および48週目から60週目までの最高矯正視力文字数の平均値のベースラインからの変化量は、8mg12週間隔投与群でそれぞれ+6.9文字、+6.8文字、8mg16週間隔投与群でそれぞれ+6.2文字、+6.4文字、2mg8週間隔投与群でそれぞれ+7.8文字、+7.8文字でした。
最高矯正視力文字数の平均値のベースラインからの変化量(中間事象※前のOC、FAS)

最高矯正視力文字数の平均値(中間事象※前のOC、FAS)
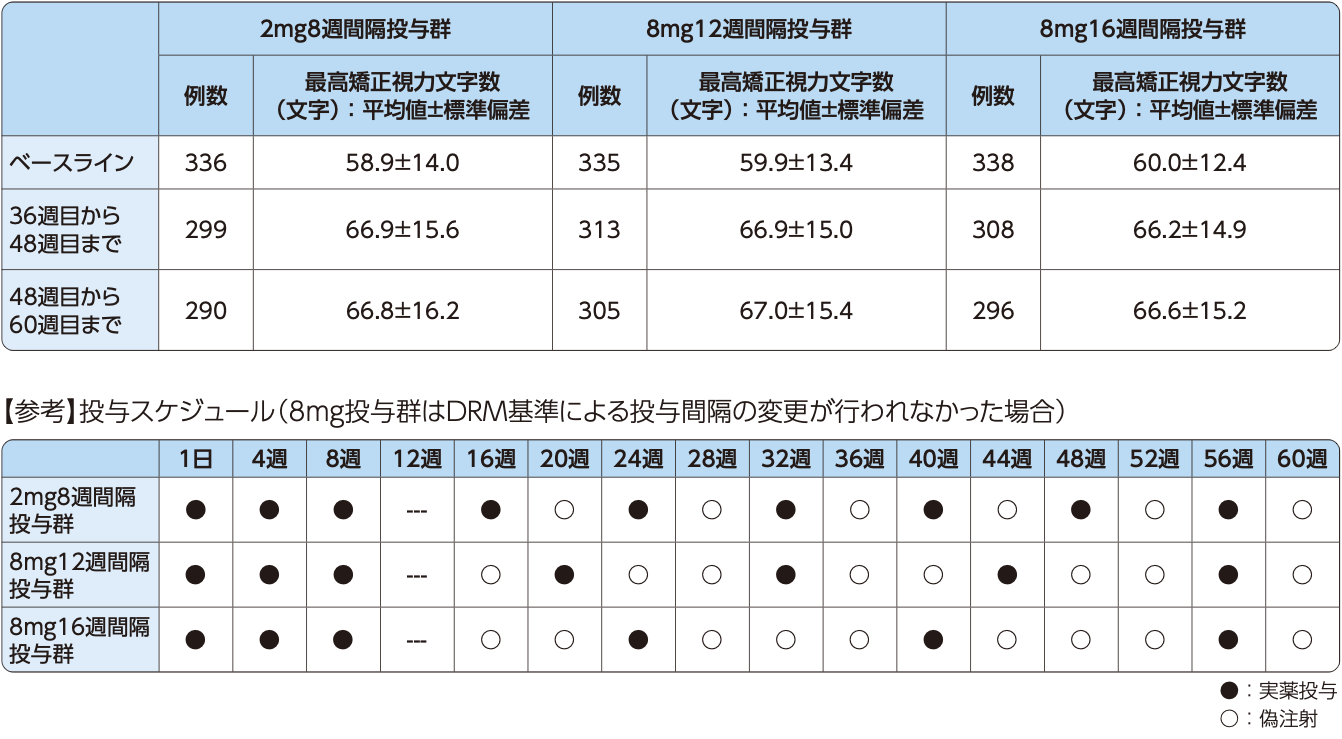
※ 試験薬の投与中止など
OC(observed case)
形態学的評価
16週目に中心窩領域にIRFおよびSRFが認められなかった患者の割合[主な副次評価項目]
16週目に中心窩領域にIRFおよびSRFが認められなかった患者の割合について、8mg投与群併合と2mg8週間隔投与群との群間差(両側95%信頼区間)は11.7(5.3, 18.2)%であり、8mg投与群併合の2mg8週間隔投与群に対する優越性が示されました。
中心窩領域にIRFおよびSRFが認められなかった患者の割合(LOCF、FAS)

※1
8mg投与群併合‒2mg8週間隔投与群[地域(日本、その他の地域)およびベースラインの最高矯正視力文字数(60文字未満、60文字以上)で層別化したMantel-Haenszel型の重みを用いて調整した]
※2
地域(日本、その他の地域)およびベースラインの最高矯正視力文字数(60文字未満、60文字以上)で調整した片側CMH検定
中心窩領域にIRFおよびSRFが認められなかった患者の割合
[48週:その他の副次評価項目、60週:探索的評価項目]
中心窩領域にIRFおよびSRFが認められなかった患者の割合は、48週目では8mg12週間隔投与群で71.1%、8mg16週間隔投与群で66.8%、2mg8週間隔投与群で59.4%でした。また、60週目ではそれぞれ74.6%、72.2%、74.6%でした。
中心窩領域にIRFおよびSRFが認められなかった患者の割合(LOCF、FAS)

※
各群‒2mg8週間隔投与群[地域(日本、その他の地域)およびベースラインの最高矯正視力文字数(60文字未満、60文字以上)で層別化したMantel-Haenszel型の重みを用いて調整した]
CNV病変面積のベースラインからの変化量
[48週:その他の副次評価項目、60週:探索的評価項目]
48週目におけるCNV病変面積のベースラインからの変化量(最小二乗平均値)は、8mg12週間隔投与群で-3.7mm2、8mg16週間隔投与群で-2.9mm2、2mg8週間隔投与群で-2.4mm2でした。また、60週目のベースラインからの変化量(平均値)はそれぞれ-3.8mm2、-3.7mm2、-3.9mm2でした。
CNV病変面積のベースラインからの変化量(FAS)

※1 実測値 ※2 各群‒2mg8週間隔投与群
●
MMRM:ベースラインのCNV病変面積を共変量、投与群、来院および層別因子[地域(日本、その他の地域)、ベースラインの最高矯正視力文字数(60文字未満、60文字以上)]を固定効果とし、ベースラインのCNV病変面積と来院の交互作用項、投与群と来院の交互作用項を含む。
CRTのベースラインからの変化量[48週:その他の副次評価項目、60週:探索的評価項目]
CRTのベースラインからの変化量(最小二乗平均値)は、48週目では8mg12週間隔投与群で-147.4μm、8mg16週間隔投与群で-146.8μm、2mg8週間隔投与群で-136.3μmでした。また、60週目ではそれぞれ-153.7μm、-150.7μm、-154.8μmでした。
CRTのベースラインからの変化量(MMRM、FAS)

※1 実測値 ※2 各群‒2mg8週間隔投与群
CRTのベースラインからの変化量の推移(MMRM、FAS)

●
MMRM:ベースラインのCRTを共変量、投与群、来院および層別因子[地域(日本、その他の地域)、ベースラインの最高矯正視力文字数(60文字未満、60文字以上)]を固定効果とし、ベースラインのCRTと来院の交互作用項、投与群と来院の交互作用項を含む。
投与に関する評価
48週目まで投与間隔が12週間隔以上であった患者の割合/
投与間隔が16週間隔以上であった患者の割合[探索的評価項目]
8mg12週間隔投与群において48週目まで投与間隔が12週間隔であった患者の割合は79.4%、8mg16週間隔投与群において48週目まで投与間隔が16週間隔であった患者の割合は76.6%でした。
8mg12週間隔投与群における48週目までの最終投与間隔の分布(SAF※)

※ SAFのうち48週目までの投与を完了した患者のみ
8mg16週間隔投与群における48週目までの最終投与間隔の分布(SAF※)

48週目までに投与間隔が短縮となった患者の割合/次回予定された投与間隔別の患者の割合
[事前に規定されたその他の評価項目]
48週目までに投与間隔が短縮となった患者の割合、次回予定された投与間隔別の患者の割合(SAF※1)

例数(%)
※1 SAFのうち48週目までの投与を完了した患者のみ
※2 48週目までの最終来院日における評価に基づく投与間隔
60週目まで投与間隔が12週間隔以上であった患者の割合/
投与間隔が16週間隔以上であった患者の割合[探索的評価項目]
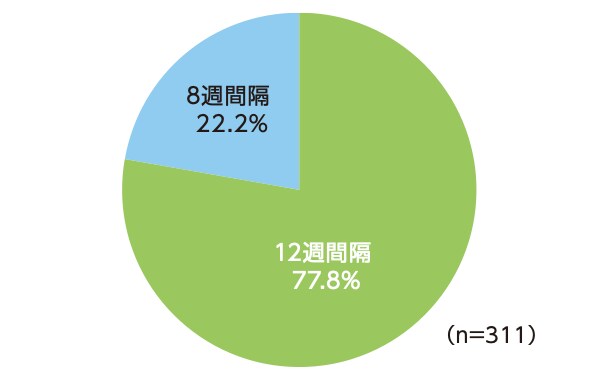
8mg12週間隔投与群において60週目まで投与間隔が12週間隔であった患者の割合は77.8%、8mg16週間隔投与群において60週目まで投与間隔が16週間隔であった患者の割合は74.1%でした。
8mg12週間隔投与群における60週目までの最終投与間隔の分布(SAF※)
※ SAFのうち60週目までの投与を完了した患者のみ
8mg16週間隔投与群における60週目までの最終投与間隔の分布(SAF※)

60週目までに投与間隔が短縮となった患者の割合/次回予定された投与間隔別の患者の割合
[事前に規定されたその他の評価項目]
60週目までに投与間隔が短縮となった患者の割合、次回予定された投与間隔別の患者の割合(SAF※1)

例数(%)
※1 SAFのうち60週目までの投与を完了した患者のみ
※2 60週目までの最終来院日における評価に基づく投与間隔
48週目および60週目までの投与回数[事前に規定されたその他の評価項目]
試験眼に対する投与回数(平均値)は、48週目では8mg12週間隔投与群で5.9回、8mg16週間隔投与群で5.1回、2mg8週間隔投与群で6.7回、60週目ではそれぞれ6.9回、6.0回、8.5回でした。
投与回数※1(試験眼、SAF)

※1 偽注射を除く投与回数
※2 SAF(n=338)のうち1例が欠測
安全性
有害事象[60週間]
PULSAR試験(60週間)において、すべての有害事象は8mg12週間隔投与群で335例中256例(76.4%)、8mg16週間隔投与群で338例中273例(80.8%)、2mg8週間隔投与群で336例中260例(77.4%)に認められました。
主な有害事象は、8mg12週間隔投与群でCOVID-19、高血圧が各19例(5.7%)、白内障16例(4.8%)、背部痛15例(4.5%)、上咽頭炎14例(4.2%)、視力低下13例(3.9%)、網膜出血12例(3.6%)、網膜下液、眼圧上昇が各11例(3.3%)、関節痛10例(3.0%)、8mg16週間隔投与群でCOVID-19が31例(9.2%)、上咽頭炎21例(6.2%)、視力低下20例(5.9%)、高血圧18例(5.3%)、白内障15例(4.4%)、硝子体浮遊物、背部痛が各14例(4.1%)、網膜出血、尿路感染が各13例(3.8%)、無症候性COVID-19が11例(3.3%)、硝子体剥離、眼圧上昇が各10例(3.0%)、2mg8週間隔投与群で視力低下21例(6.3%)、背部痛18例(5.4%)、COVID-19、上咽頭炎が各16例(4.8%)、網膜出血15例(4.5%)、白内障、硝子体浮遊物が各13例(3.9%)、網膜下液、尿路感染、高血圧が各12例(3.6%)でした。
試験薬に関連する重篤な有害事象は、8mg16週間隔投与群で閉塞隅角緑内障、心筋梗塞、肺塞栓症が各1例、2mg8週間隔投与群で脳血管発作が2例、急性心筋梗塞、高血圧が各1例に認められました。
試験薬に関連する投与中止に至った有害事象は、8mg16週間隔投与群で虹彩毛様体炎、網膜下液が各1例、2mg8週間隔投与群で脳血管発作が1例に認められました。
本試験において、試験薬に関連する死亡は認められませんでした。
MedDRA ver.25.0
SAF
![PULSAR試験:安全性 - 有害事象[60週間]の表](/sites/g/files/vrxlpx7866/files/2024-02/8mg_safety_namd_pulsar_img21.png)
発現例数(発現割合%)
眼内炎症反応、眼圧上昇事象、眼圧上昇の程度、高血圧事象、APTC定義による動脈血栓塞栓事象 [60週間]
アイリーア[40mg/mL(2mg)]†の臨床開発、および医薬品リスク管理計画ならびに定期的安全性最新報告で検討された項目に基づき、アイリーア8mgにおけるより詳細な検討のために追加で安全性を評価する事象‡を定義しました。評価した事象のうち、眼内炎症反応、眼圧上昇事象、眼圧上昇の程度、高血圧事象、APTC定義による動脈血栓塞栓事象の結果は、以下の通りでした。
†
未熟児網膜症以外[未熟児網膜症:濃度40mg/mL(0.4mg)]
‡
眼内炎症反応、眼圧上昇事象、網膜色素上皮裂孔事象、網膜裂孔/剥離事象、白内障事象、過敏症事象、動脈血栓塞栓事象、APTC定義による動脈血栓塞栓事象、静脈血栓塞栓事象、高血圧事象、眼以外の出血事象および鼻粘膜障害事象
SAF
![PULSAR試験:安全性 - 眼内炎症反応、眼圧上昇事象、眼圧上昇の程度、高血圧事象、APTC定義による動脈血栓塞栓事象[60週間]の表](/sites/g/files/vrxlpx7866/files/2024-02/8mg_safety_namd_pulsar_img22.png)
発現例数(発現割合%)または例数(%)
※1
MedDRA ver.25.0
※2
試験眼を対象とする
※3
投与後測定は患者が施設を離れる前の最終測定、60週目の投与後のデータは除外
※4
すべての有害事象のうち、APTC(Antiplatelet Trialists' Collaboration)定義により判定された動脈血栓塞栓事象
※5
データベースに表示されなかった1例を含む



