日本人を含む第Ⅲ相国際共同試験:MYRROR試験1)
(偽注射に対する優越性の検証)
1)バイエル薬品社内資料[日本人を含む第Ⅲ相国際共同試験:MYRROR試験]承認時評価資料
本ページでは「アイリーア(2mg)」を「アイリーア」と記載しています。
滲出型加齢黄斑変性(AMD)患者を対象とした海外第Ⅱ相試験(CLEAR-ITⅡ試験)および糖尿病黄斑浮腫(DME)患者を対象とした海外第Ⅱ相試験(706試験)の結果、ならびに他のVEGF阻害剤(ベバシズマブ、ラニビズマブ)の病的近視における脈絡膜新生血管(mCNV)における臨床研究報告を参考に、アイリーアの用法及び用量を「2mgを4週ごとに硝子体内投与する」と設定し、アイリーアの偽注射に対する優越性を検証しました。
【実施地域】
日本、韓国、台湾、香港、シンガポールの5ヵ国・地域、20施設
試験概要
目的
mCNVを有する患者を対象に、アイリーアの有効性について偽注射に対する優越性を検証するとともに、安全性および忍容性についても検討する
試験対象
mCNVを有する患者122例(うち日本人:90例)
[主な選択基準]
- 病的近視における活動性の中心窩下または傍中心窩の脈絡膜新生血管を有する18歳以上の男女
- 眼軸長26.5mm以上、または-6ディオプター以上の近視
- 試験眼のETDRS視力表による最高矯正視力文字数が73~35文字(スネレン視力で20/40~20/200) など
[主な除外基準]
- 試験眼に病的近視以外の原因によるCNVを認める、または既往歴がある
- 試験眼に他の治験薬、汎網膜光凝固術、レーザー温熱療法、光線力学的療法(PDT)による治療歴を有する
- いずれかの眼にVEGF阻害剤による治療歴または全身性のVEGF阻害剤の治療歴を有する、あるいは過去3ヵ月以内に副腎皮質ステロイド剤の眼内または眼周囲注射による治療歴を有する
- 過去6ヵ月以内に脳血管障害または心筋梗塞の既往を有する など
試験デザイン
無作為化二重遮蔽偽注射対照比較試験
投与方法
対象患者を、アイリーア群および偽注射群の2群に無作為に割り付けた。
アイリーア群は、アイリーア2mgを単回投与後、44週目まで4週ごとに再投与基準に従いアイリーア2mgの再投与または偽注射を行った。偽注射群は、偽注射を単回投与後、20週目まで4週ごとに偽注射を繰り返し、24週目にアイリーア2mgを単回投与後、44週目まで4週ごとに再投与基準に従いアイリーア2mgの再投与または偽注射を行った。
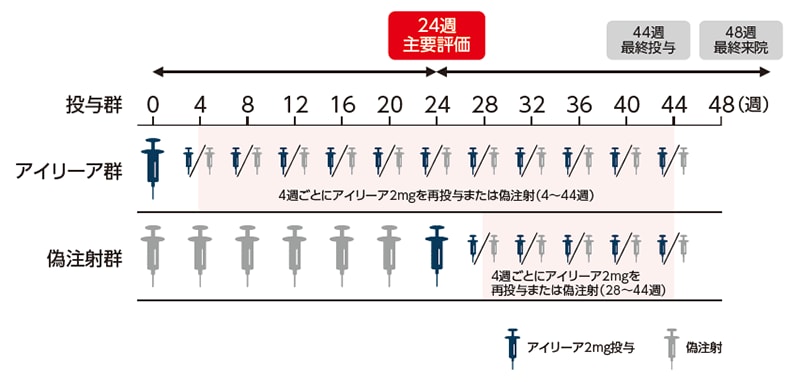
[再投与基準]
以下の基準のうち1項目以上を満たす:
- 最高矯正視力文字数が前回の検査から5文字以上低下
- 中心網膜厚(CRT)が前回の検査よりも50μm超増加
- 新規または遷延性の網膜の嚢胞性変化、網膜下液、色素上皮剥離
- 新規または遷延性の脈絡膜新生血管または出血
- 治験担当医師の印象および/または標準医療の診断から、投与が必要と考えられる場合
主な有効性評価項目
主要評価項目:
24週目における最高矯正視力文字数のベースラインからの変化量
副次評価項目:
24週目にベースラインから15文字以上の視力改善がみられた患者の割合
探索的評価項目:
24週目および48週目までの各観察時点における最高矯正視力文字数のベースラインからの変化量
24週目および48週目までの各観察時点における5、10または15文字以上の視力改善または視力低下がみられた患者の割合
24週目および48週目におけるCRTのベースラインからの変化量
24週目および48週目におけるCNV病変サイズのベースラインからの変化量
24週目および48週目におけるFAによる蛍光漏出量のベースラインからの変化量
24週目および48週目におけるNEI VFQ-25合計スコアのベースラインからの変化量 など
主な安全性評価項目
有害事象、副作用、重篤な有害事象、投与中止に至った有害事象、死亡、APTC定義による動脈血栓塞栓事象 など
解析計画
検証的な解析(第1種の過誤を考慮し、検出力を考慮し例数設計された解析)
- 主要評価項目(FAS):アイリーア投与群の偽注射群に対する優越性の検証
第1種の過誤を考慮した解析(検出力を考慮した例数設計はされていない)
- 副次評価項目(FAS):同上。ただし主要評価項目で優越性が検証された場合に限り実施
探索的な解析
- 探索的評価項目(FAS)
部分集団解析:日本人の部分集団解析 など
mCNV(myopic choroidal neovascularization):病的近視における脈絡膜新生血管
FAS(full analysis set):最大の解析対象集団
FA(fluorescein angiography):フルオレセイン蛍光眼底造影
NEI VFQ-25(National Eye Institute 25-item Visual Function Questionnaire):米国国立眼病研究所の25項目からなる視覚機能についてのアンケート
●
偽注射:硝子体内注射と同じ処置を行うが、注射の代わりに針のない注射シリンジを局所麻酔下で眼球に押し付ける方法
病的近視における脈絡膜新生血管の用法及び用量
アフリベルセプト(遺伝子組換え)として1回あたり2mg(0.05mL)を硝子体内投与する。投与間隔は、1ヵ月以上あけること。
試験対象例数と各群の患者の内訳

※ 偽注射群では24週目以降アイリーア投与
患者背景および特性(FAS)
MYRROR試験において、各投与群のベースライン時の人口統計学的特性は以下の通りでした。

視力評価
(1)視力の変化
24週目における最高矯正視力文字数のベースラインからの変化量は、アイリーア群で+12.1文字であったのに対し、偽注射群では-2.0文字であり、アイリーア群の偽注射群に対する優越性が検証されました。また、48週目における最高矯正視力文字数のベースラインからの変化量は、アイリーア群では+13.5文字、偽注射群では+3.9文字でした。
最高矯正視力文字数の変化量の推移(LOCF、FAS)

※1
投与群および国を固定効果、最高矯正視力文字数のベースライン値を共変量としたANCOVAモデル
※2
アイリーア群-偽注射群
LOCF(last observation carried forward):最終評価スコア外挿法
(2)視力の改善
24週目にベースラインから15文字以上の視力改善がみられた患者の割合は、アイリーア群では38.9%、偽注射群では9.7%であり、アイリーア群の偽注射群に対する優越性が示されました。48週目にベースラインから15文字以上の視力改善がみられた患者の割合はアイリーア群では50.0%であり、24週目にアイリーアの投与が開始された偽注射群では29.0%でした。
15文字以上の視力改善がみられた患者の割合(LOCF、FAS)

※1
24週目以降アイリーア投与
※2
国で調整した両側CMH検定
※3
アイリーア群-偽注射群(国を層としたCMH型の重みを用いて調整した)
形態学的評価
(1)中心網膜厚(CRT)の変化
アイリーア群のCRTの変化量は、24週目に-79.1μm、48週目に-83.1μmと推移しました。一方、偽注射群のCRTの変化量は、24週目に-4.2μm、48週目に-56.7μmでした。
CRTの変化量の推移(LOCF、FAS)

※1
投与群および国を固定効果、CRTのベースライン値を共変量としたANCOVAモデル
※2
アイリーア群-偽注射群
(2)脈絡膜新生血管(CNV)病変サイズの変化
CNV病変サイズの変化量(LOCF、FAS):探索的評価項目

※1
24週目以降アイリーア投与
※2
投与群および国を固定効果、CNV病変サイズのベースライン値を共変量としたANCOVAモデル
※3
アイリーア群-偽注射群
(3)フルオレセイン蛍光眼底造影(FA)による蛍光漏出量の変化
FAによる蛍光漏出量の変化量(LOCF、FAS):探索的評価項目

※1
24週目以降アイリーア投与
※2
投与群および国を固定効果、FAによる蛍光漏出量のベースライン値を共変量としたANCOVAモデル
※3
アイリーア群-偽注射群
QOLに関する評価
【参考情報】NEI VFQ-25合計スコア
NEI VFQ-25合計スコアの変化量(LOCF、FAS):探索的評価項目

※1
24週目以降アイリーア投与
※2
投与群および国を固定効果、NEI VFQ-25合計スコアのベースライン値を共変量としたANCOVAモデル
※3
アイリーア群-偽注射群
安全性(48週間の有害事象発現率)
MYRROR試験(48週間)において、すべての有害事象はアイリーア群で91例中64例(70.3%)、偽注射群で31例中18例(58.1%)に認められました。主な有害事象はアイリーア群で鼻咽頭炎17例(18.7%)、結膜出血10例(11.0%)、偽注射群で点状角膜炎4例(12.9%)などでした。副作用※1は、アイリーアを投与された116例※2中25例(21.6%)に認められました。主な副作用は、結膜出血10例(8.6%)、点状角膜炎7例(6.0%)、眼痛6例(5.2%)などでした。試験薬に関連する重篤な有害事象は、アイリーア群で黄斑円孔が1例に認められました。試験薬に関連する投与中止に至った有害事象および試験薬に関連する死亡は認められませんでした。
※1
投与手技に起因する有害事象を含む
※2
アイリーア群91例、偽注射群25例
MYRROR試験

発現例数(発現率%)
a)
0~20週目は4週ごとに偽注射を行い、24週目にアイリーアを単回投与後、28~44週目は4週ごとにアイリーア投与または偽注射を行った
b)
すべての有害事象のうち、APTC(Antiplatelet Trialists’ Collaboration)定義により判定された動脈血栓塞栓事象



