国内第Ⅲ相試験:VEGA試験1)(偽注射に対する優越性の検証)、
VENERA試験2)(VEGA試験の有効性の確認)
1)バイエル薬品社内資料[国内第Ⅲ相試験:VEGA試験]承認時評価資料
2)バイエル薬品社内資料[国内第Ⅲ相試験:VENERA試験]承認時評価資料
アイリーア(2mg)の承認された効能又は効果(抜粋):血管新生緑内障
本ページでは、「アイリーア(2mg)」を「アイリーア」と記載しています。
VEGA試験では、偽注射に対するアイリーアの優越性を検証できなかったため、その要因を考慮して計画したVENERA試験を追加で実施しました。
【実施地域】
VEGA試験:日本、19施設 VENERA試験:日本、7施設
試験概要
目的
血管新生緑内障(NVG)患者におけるアイリーアの有効性について眼圧の変化を用いて検討し、安全性および忍容性についても検討する
試験対象
NVGを有する患者 VEGA試験:54例、VENERA試験:16例
[主な選択基準]
虹彩新生血管(NVI)および隅角新生血管(NVA)が認められ、それに伴い試験眼の眼圧が25mmHgを超えている成人NVG患者
[主な除外基準(VEGA試験、VENERA試験共通)]
- NVG以外の原因による閉塞隅角を有する
- 試験眼に、初回投与日の前60日以内にVEGF阻害剤の治療歴を有する
- 試験眼またはその周囲に、初回投与日の前60日以内に副腎皮質ステロイド剤〔溶液(非懸濁液)または懸濁液〕の治療歴を有する(副腎皮質ステロイド点眼薬は可)
- 試験眼に、PRPを除く有効性評価に影響を与える眼内手術歴を有する など
相違点
[VEGA試験の除外基準]
- 初回投与日の投与前に行う眼圧評価の前24時間以内に、全身性の眼圧下降薬の治療歴を有する
- 試験眼に、初回投与日の前30日以内にPRPを除く有効性評価に影響を与える眼内手術以外の眼内手術の治療歴を有する
- 試験眼に、初回投与日の後15日以内にPRPを除くすべての眼内手術が予定されている
[VENERA試験の除外基準]
- 初回投与日の前3日以内に、全身性の眼圧下降薬の治療歴を有する
- 試験眼に、初回投与日の前30日以内にPRPを含む有効性評価に影響を与える眼内手術以外の眼内手術の治療歴を有する
- 試験眼に、初回投与日の後8日以内にPRPを含むすべての眼内手術が予定されている
- NVGが原因の完全閉塞隅角を有する
試験デザイン
VEGA試験:無作為化二重遮蔽偽注射対照比較試験
VENERA試験:非無作為化非遮蔽単群試験
投与方法
<VEGA試験>
対象患者を、アイリーア群および偽注射群の2群に無作為に割り付けた。初回投与日(1日目)にアイリーア群ではアイリーア2mgを単回硝子体内投与し、偽注射群では偽注射を行った。その後、2週目および13週目を除く各来院時に再投与基準を満たした場合のみ、1週目にはアイリーア群に偽注射、偽注射群にアイリーア2mg投与を行い、5週目および9週目にはいずれの投与群でもアイリーア2mg投与を行った

[VEGA試験における再投与基準]
以下の基準のすべてを満たす:
- 眼圧が21mmHg超
- NVIの退縮が不十分(NVIグレードが0以外)
- アイリーアの硝子体内投与が必要であると治験担当医師が判断した場合
<VENERA試験>
初回投与日(1日目)にアイリーア2mgを単回硝子体内投与し、1週目および2週目に、検査を行った。患者は5週目に来院し、試験終了時の検査を行った。

主な有効性評価項目
主要評価項目:
1週目における眼圧のベースラインからの変化量
副次評価項目:
1週目におけるNVIグレードがベースラインと比較して改善した患者の割合
探索的評価項目:
各来院時点における眼圧のベースラインからの変化量、各来院時点において眼圧をコントロール(≦21mmHg)できた患者の割合、各来院時点においてNVIおよびNVAグレードがベースラインと比較して改善した患者の割合、各来院時点におけるNVIおよびNVAグレードの割合 など
主な安全性評価項目
有害事象、副作用、重篤な有害事象、投与中止に至った有害事象、死亡、APTC定義による動脈血栓塞栓事象 など
解析計画
検証的な解析
VEGA試験:
主要評価項目(FAS):アイリーア群の偽注射群に対する優越性の検証(変化量の調整済平均の群間差の両側95%信頼区間の上限が0を下回る)
VENERA試験:
主要評価項目(PPS):アイリーア群の有効性の検証(両側95%信頼区間の上限が閾値[0mmHg]を下回る)
探索的な解析
主要評価項目の補足的解析(VEGA試験:PPS)
副次評価項目(VEGA試験:FAS、VENERA試験:PPS)
探索的評価項目(VEGA試験:FAS、VENERA試験:PPS) など
事後部分集団解析†
VEGA試験における全身性眼圧下降薬使用の有無別の解析 など
† 本事後部分集団解析は、承認審査過程において評価を受けた解析です。
●偽注射:硝子体内注射と同じ処置を行うが、注射の代わりに針のない注射シリンジを局所麻酔下で眼球に押し付ける方法
NVG(neovascular glaucoma):血管新生緑内障
NVI(neovascularization of the iris):虹彩新生血管
NVA(neovascularization of the angle):隅角新生血管
VEGF(vascular endothelial growth factor):血管内皮増殖因子
PRP(panretinal photocoagulation):汎網膜光凝固
FAS(full analysis set):最大の解析対象集団
PPS(per protocol set):治験実施計画書に適合した解析対象集団
参考) NVIおよびNVAグレードa、b)
NVIおよびNVAの発現の有無について、細隙灯顕微鏡と隅角鏡検査により評価しました。試験眼におけるNVI およびNVAの程度は、以下に示すスコア表に従ってスコア化しました。
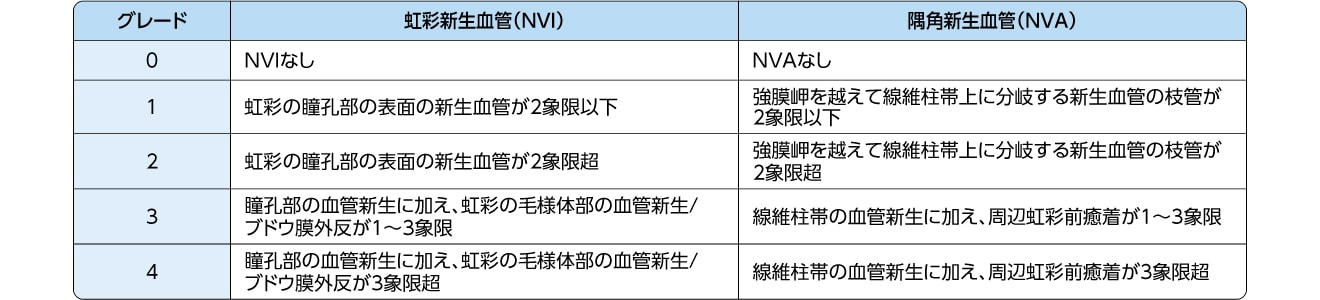
a) Weiss DI, et al.: Ann Ophthalmol 1978; 10: 488-491.
b) Teich SA, et al.: Ophthalmology 1981; 88: 1102-1106.
眼圧の変化及び推移:VEGA試験、VENERA試験
眼圧の変化:VEGA試験

- VEGA試験での主要評価項目において、アイリーアの偽注射に対する優越性は検証されませんでした
- なお、PPSを対象とした補足的解析ではアイリーアの有効性が示唆されました
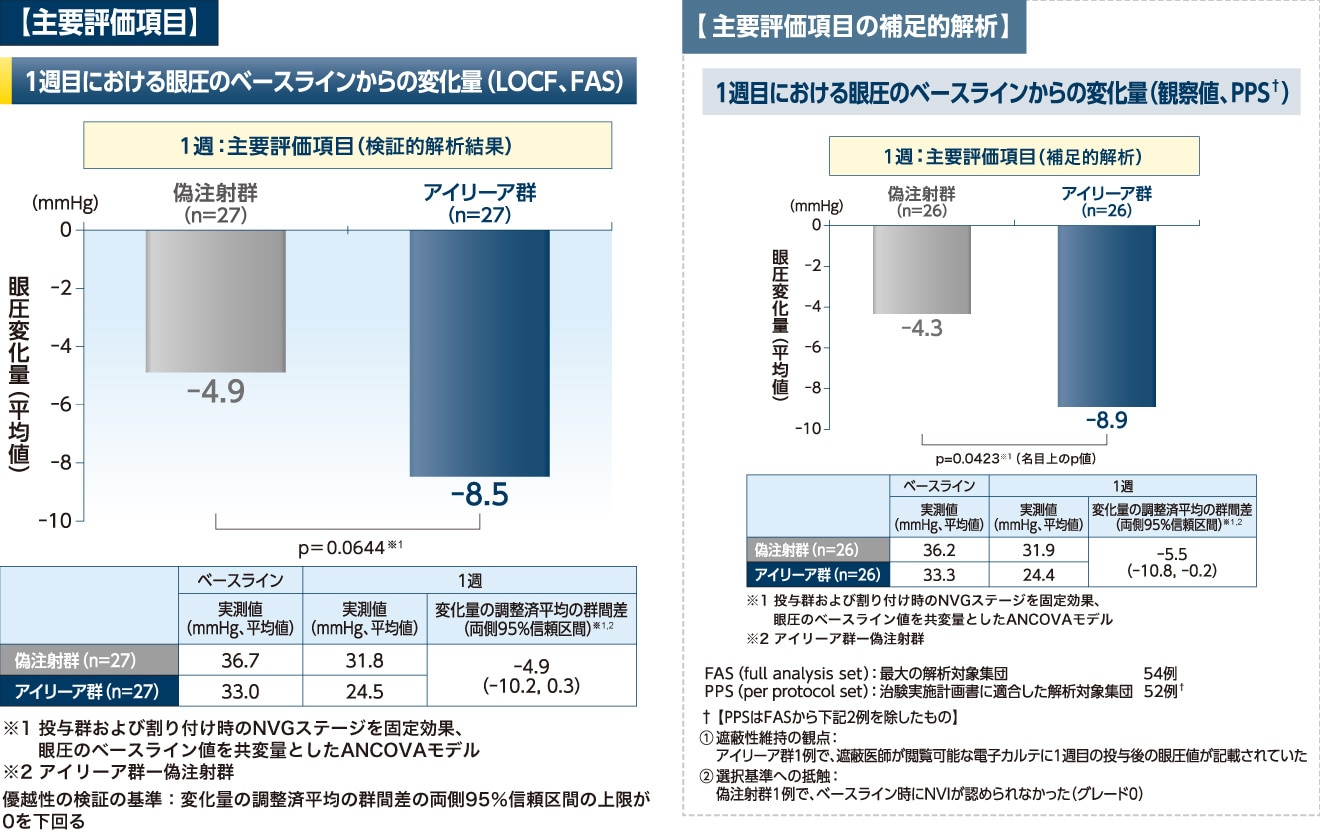
LOCF(last observation carried forward):最終評価スコア外挿法
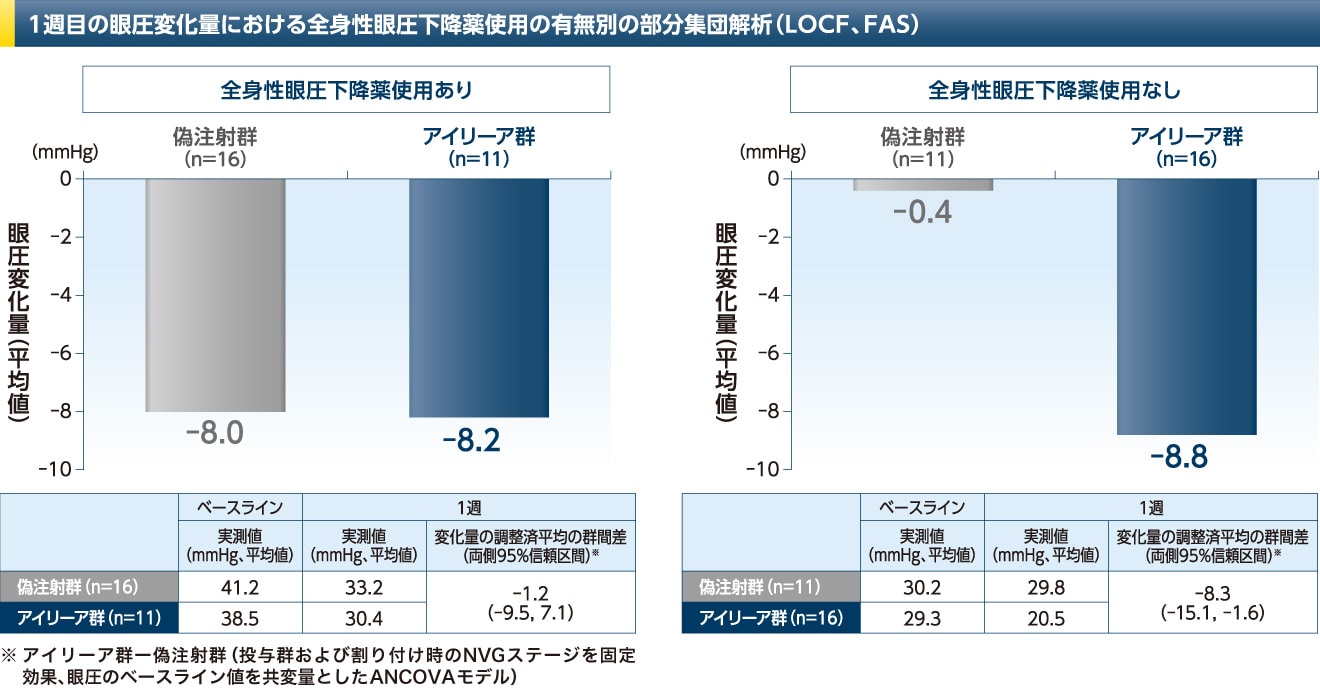
<事後部分集団解析>

- 全身性眼圧下降薬の使用*によって、1週目の偽注射群においても眼圧下降(-8.0mmHg)が生じたことが、アイリーア群の偽注射群に対する統計学的優越性が示されなかった原因である可能性が考えられました
- なお、本事後解析の結果を踏まえて、追加試験であるVENERA試験が設計されました
* ベースラインから1週目の投与前に行う眼圧評価の24時間前までの期間における全身性眼圧下降薬の使用
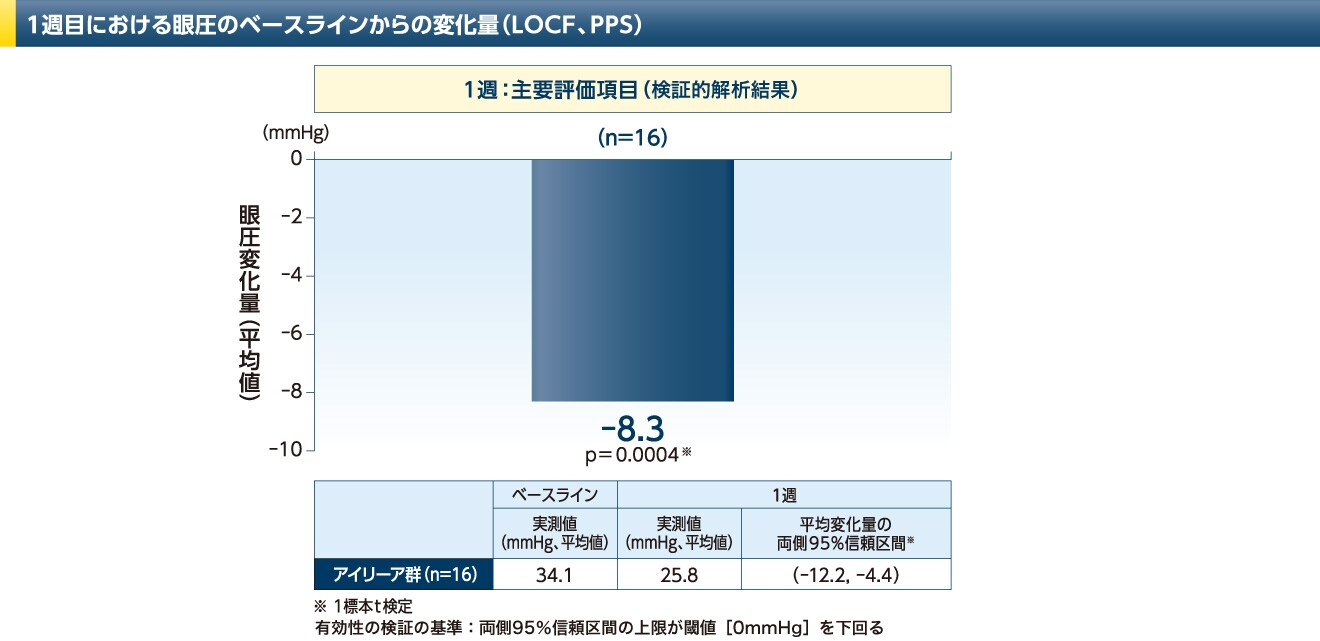
眼圧の変化:VENERA試験

- VENERA試験では、主要評価項目である1週目における眼圧のベースラインからの変化において、アイリーアの有効性が検証されました
眼圧の推移:VEGA試験、VENERA試験
<探索的評価項目>
- VEGA試験では、最終評価時(13週目)における眼圧のベースラインからの変化量の平均値は、アイリーア群で-13.4mmHg、偽注射群†で-18.6mmHgでした
- VENERA試験では、最終評価時(5週目)における眼圧のベースラインからの変化量の平均値は、-15.5mmHgでした

虹彩・隅角新生血管の評価
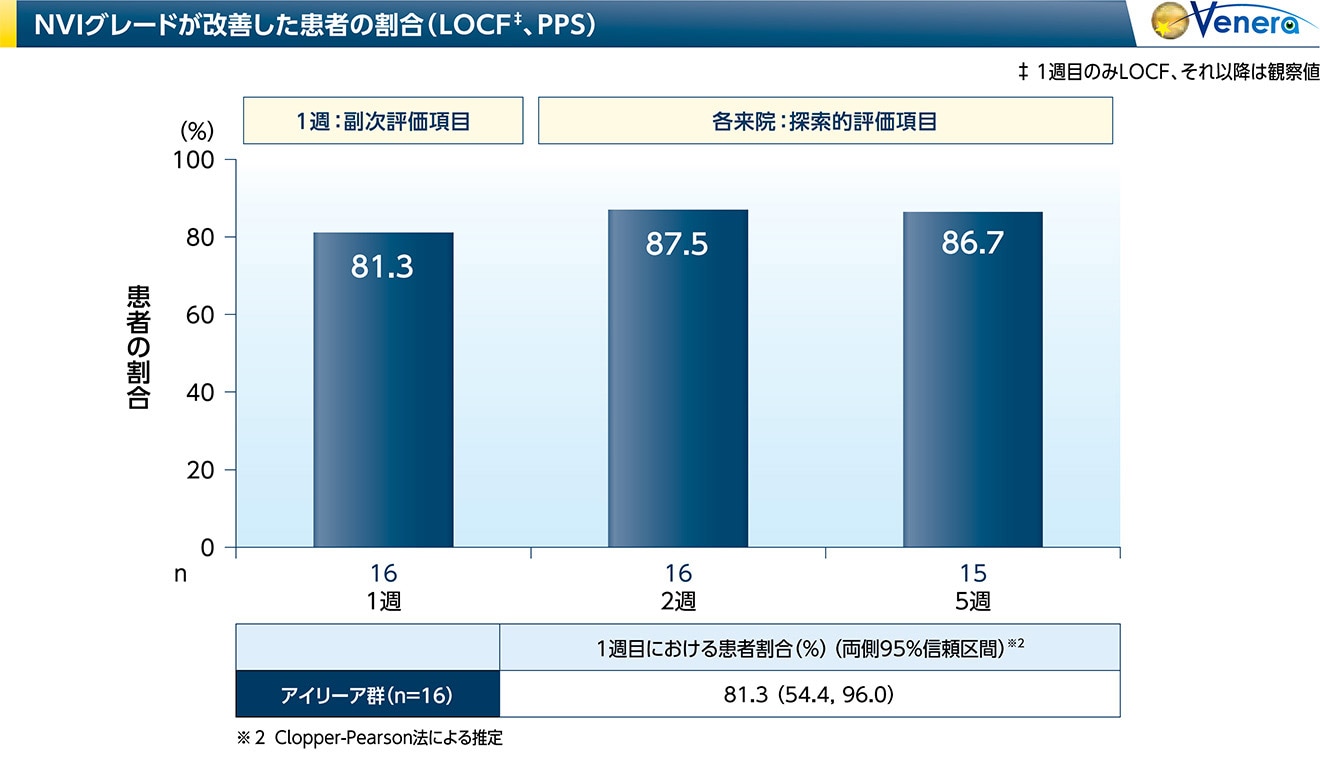
虹彩新生血管(NVI)グレードの改善*:VEGA試験、VENERA試験
<副次評価項目>
- VEGA試験では、1週目に眼圧上昇の原因となるNVIが改善*した患者の割合は、アイリーア群で70.4%、偽注射群で11.5%でした
- VENERA試験では、1週目に眼圧上昇の原因となるNVIが改善*した患者の割合は、81.3%でした
* 改善の定義:ベースラインと比較して少なくとも1段階の改善

隅角新生血管(NVA)グレードの改善*:VEGA試験、VENERA試験
<探索的評価項目>
- VEGA試験では、1週目に眼圧上昇の原因となるNVAが改善*した患者の割合は、アイリーア群で59.3%、偽注射群で11.5%でした
- VENERA試験では、1週目に眼圧上昇の原因となるNVAが改善*した患者の割合は、50.0%でした
* 改善の定義:ベースラインと比較して少なくとも1段階の改善


安全性:VEGA試験、VENERA試験
VEGA試験(13週間)において、副作用※はアイリーアを投与された50例(アイリーア群27例、偽注射群†23例)中12例(24.0%)に認められ、VENERA試験(5週間)において、副作用※は16例中3例(18.8%)に認められました
VEGA試験(13週間)における副作用※および有害事象

副作用発現率
アイリーア群:27例中7例(25.9%)
偽注射群†:27例中5例(18.5%)
副作用の内訳
アイリーア群:結膜出血2例(7.4%)、注射部位疼痛2例(7.4%)、点状角膜炎、視力障害、角膜擦過傷が各1例(3.7%)
偽注射群†:心筋虚血、結膜出血、前房出血、網膜出血、注射部位疼痛、眼圧上昇、頭痛が各1例(3.7%)
試験薬に関連する重篤な有害事象
偽注射群†:心筋虚血1例
試験薬に関連する投与中止に至った有害事象および試験薬に関連する死亡
本試験においては認められなかった
†1週目以降、再投与基準に従ってアイリーア2mg投与を実施
VENERA試験(5週間)における副作用※および有害事象

副作用発現率
16例中3例(18.8%)
副作用の内訳
眼痛2例(12.5%)、眼そう痒症および頭痛が各1例(6.3%)
試験薬に関連する重篤な有害事象、
試験薬に関連する投与中止に至った有害事象および試験薬に関連する死亡
本試験においては認められなかった
※投与手技に起因する有害事象を含む。



